Le bermekimab est un anticorps monoclonal dirigé contre l’interleukine 1 α. Cette interleukine est très présente dans les kératinocytes. Beaucoup de cellules possèdent des récepteurs à l’anti-IL 1α dans l’organisme. Parmi les effets de cette interleukine, sont connues : la potentialisation de la sensation douloureuse et du prurit, la production de métalloprotéases, la néoangiogénèse et l’induction d’un infiltrat inflammatoire dans la peau. Cet anticorps ne se lie pas à la sous unité β de l’interleukine-1 (comme l’anakinra par exemple).
Cette molécule est actuellement en développement dans 5 pathologies.
Lors de cette session étaient présentés des résultats de phase 2 dans le domaine de la dermatite atopique et de la maladie de Verneuil.
Pour la dermatite atopique, sont présentés les résultats d’une étude de phase 2, ouverte, à propos de 38 patients. Le bermekimab était administré par voie sous-cutanée à la posologie de 200 mg/semaine pendant 4 semaines ou 300 mg/semaine pendant 7 semaines.
Au total, 70 % des patients ont obtenu une réponse EASI 75 à la semaine 7 dans le groupe 300 mg, et le SCORAD était diminué en moyenne de 65 % .
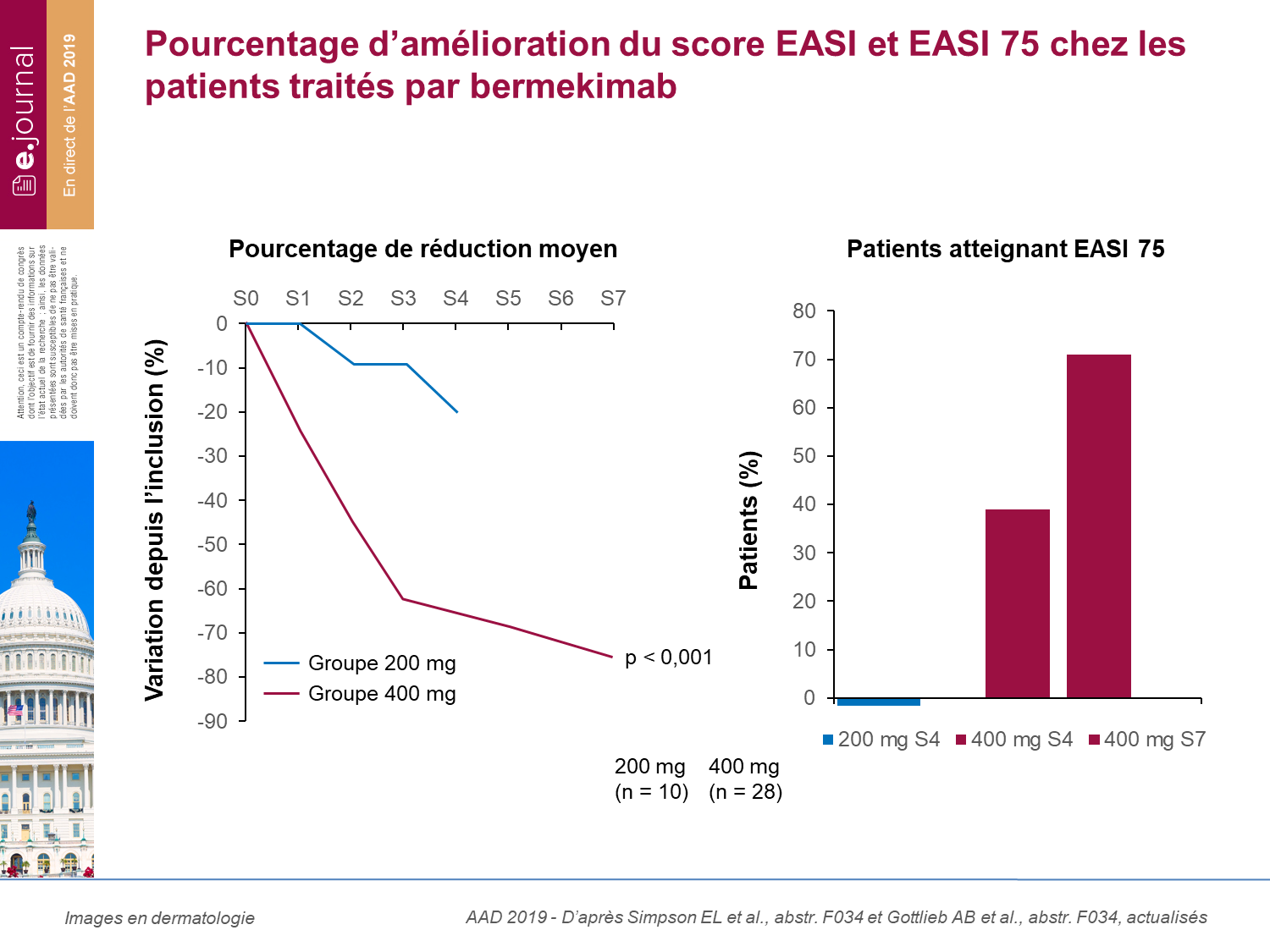
Ce traitement semble avoir des effets très intéressants sur la douleur et sur le prurit avec une amélioration importante de ces paramètres dans cette étude : diminution en moyenne de 70 % du prurit à la semaine 7 dans le bras 300 mg (évaluation par une échelle visuelle analogique), et de 85 % de la douleur chez les mêmes patients (évaluation EVA). La tolérance était bonne avec cependant des réactions au point d’injection rapportées. Devant ces résultats prometteurs d’autres études vont débuter.
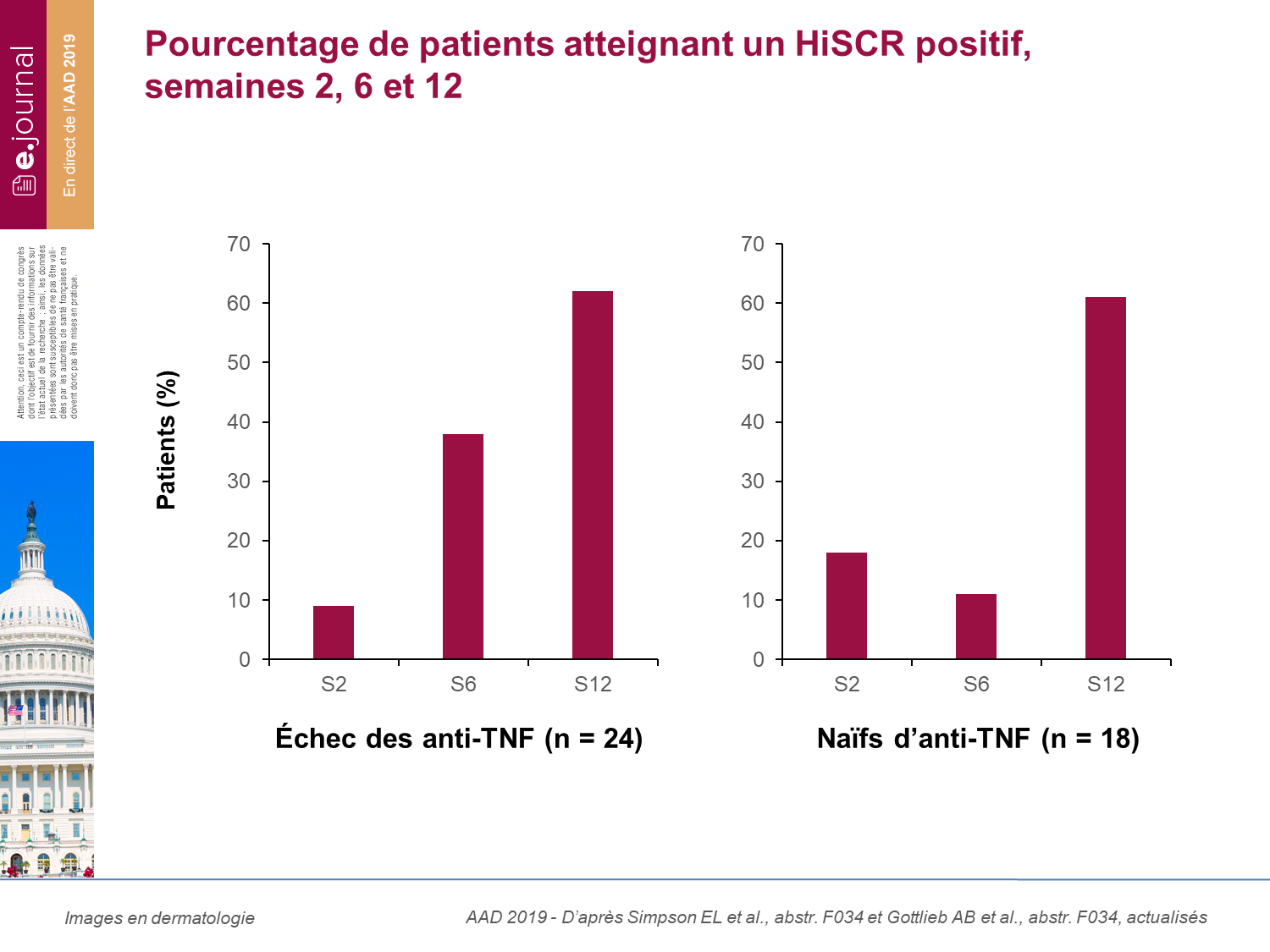
Dans le domaine de la maladie de Verneuil, le bermekimab a été étudié dans une étude ouverte de phase 2 sur 42 patients, à la dose de 400 mg /semaine pendant 12 semaines. Les patients étaient répartis en deux bras : patients en échec d’anti-TNF (n = 24) et patients naïfs d’anti-TNF (n = 18).
La réponse était évaluée par le HiSCR (Hidradenitis suppurative Clinical response) qui est positif si est observée une diminution de 50 % du nombre d’abcès et de nodules sans apparition de nouvel abcès ou fistule.
A la semaine 12, 60 % des patients avait un HiSCR positif dans les deux bras, avec une diminution de plus de 50 % de la douleur et une amélioration du DLQI de 40 % chez les patients en échec d’anti-TNF et 65 % chez les patients naïfs d’anti-TNF.
Le profil de tolérance était bon. Des essais de phase 3 vont également avoir lieu avec le bermekimab dans la maladie de Verneuil.