Méta-analyse des cellules CAR T anti-BCMA dans le myélome multiple
L’intérêt pour l’immunothérapie dans la prise en charge du myélome multiple (MM) est croissant depuis plusieurs années. L’EBMT 2020 a été l’occasion de présenter une méta-analyse évaluant les cellules CAR T anti-BCMA dans le MM.
Au total, 20 études (10 réalisées aux États-Unis/Europe et 10 en Chine) ont été inclues pour un total de 447 patients (âge médian : 60 ans) souffrant d'un MM en rechute réfractaire (R/R) lourdement prétraité (nombre médian de lignes de traitement préalables : États-Unis/Europe, n = 8 ; Chine, n = 5). De plus, 90 % des patients avaient reçu une autogreffe préalable et 35 % des patients avaient une localisation extramédullaire de la maladie lors de l’administration des CAR. Le suivi médian était très variable d’une étude à l’autre (1,1 à 12,6 mois). En revanche, les choses étaient plus homogènes en ce qui concerne le domaine de costimulation utilisé dans la CAR (4-1BB dans la majorité des études) et le traitement de lymphodéplétion utilisé (fludarabine + cyclophosphamide sauf une étude cyclophosphamide + busulfan et une étude cyclophosphamide seule). Le taux de réponse globale avec les cellules CAR T anti-BCMA est de 84 % (78-89 %) et le taux de réponse complète est de 36 % (24-50 %), avec une durée médiane de réponse de 11 mois (tableau). L’administration d’un nombre plus important de cellules CAR T anti-BCMA était associée à un taux de réponse globale et de réponse complète plus élevé (92 % (82-98 %) et 43 % (32-53 %), respectivement). L’utilisation des cellules CAR T anti-BCMA ne semble pas gommer l’impact pronostique de la cytogénétique avec un taux de réponse globale plus faible chez les patients ayant une cytogénétique à haut risque (68 % (50-81 %)). En revanche, la présence de localisations extramédullaires de la maladie n’a pas d’impact sur la réponse (78 % (47-93 %) de réponse globale). Le devenir des patients a pu être analysé sur seulement 5 études publiées ; le taux de rechute est important, 45 % (27-46 %), chez les patients répondeurs. Cependant, la survie sans progression médiane est de 10 mois et la survie globale de 84 % (60-95 %) au dernier suivi (médiane de suivi : 10 mois), ce qui reste encourageant chez des patients aussi lourdement prétraités. Finalement, 73 % (57-84 %) des patients ont fait un syndrome de relargage cytokinique (SRC), 15 % (9-23 %) un SRC de grade 3-4, et 17 % (10-27 %) une neurotoxicité.
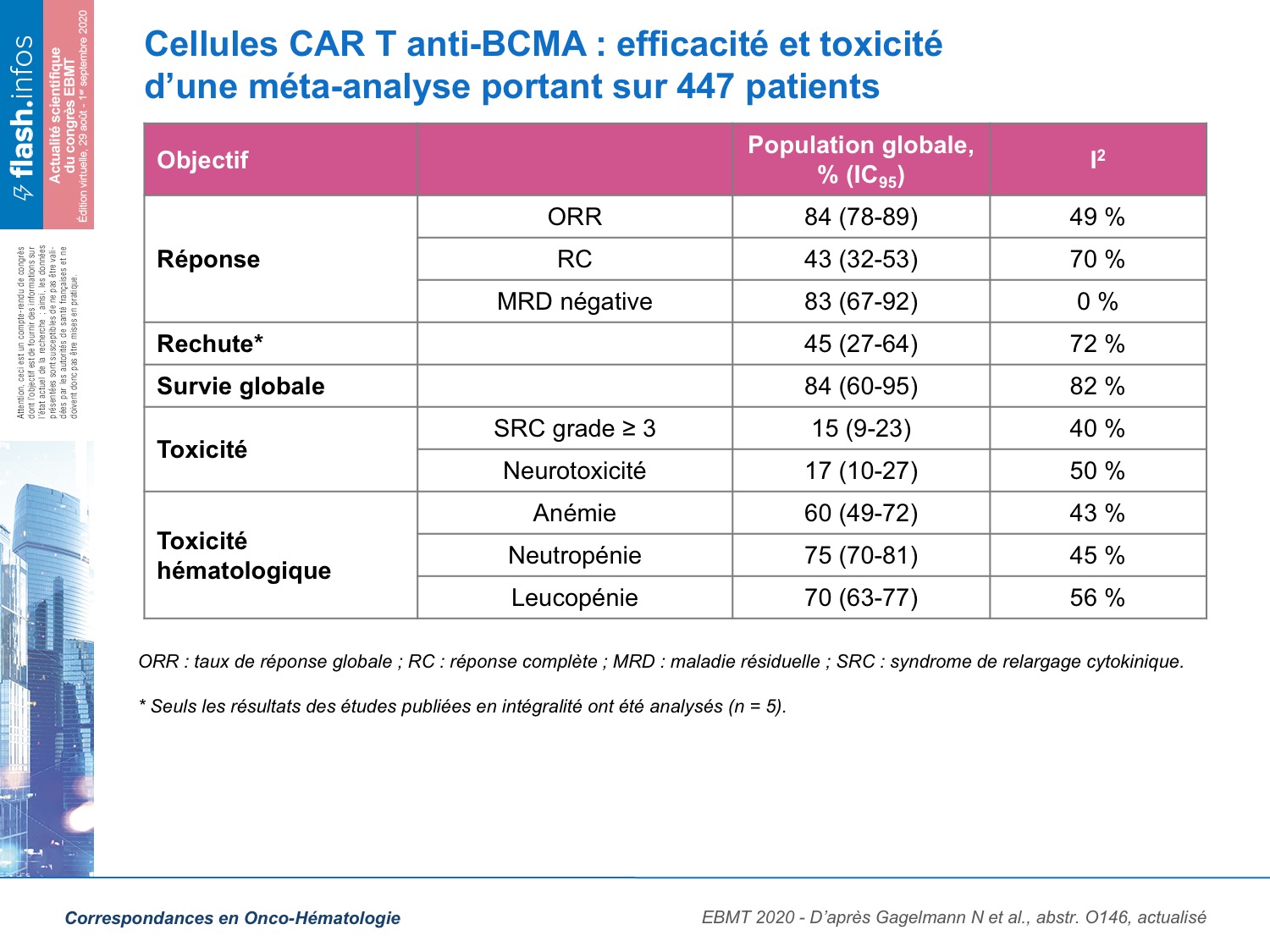
Cette méta-analyse révèle que les cellules CAR T anti-BCMA sont associées à des taux de réponse élevés et à une toxicité modérée dans le MM R/R et très lourdement prétraité. Cependant, le taux de rechute reste élevé : presque la moitié des répondeurs. Des études évaluant leur utilisation plus précoce, avec un suivi plus long semblent donc indispensables pour définir la place exacte de cette nouvelle stratégie thérapeutique dans la prise en charge du MM.






