Carboplatine + étoposide versus topotecan en 2e ligne dans le CBPC ‟sensible” : une étude randomisée de phase III
Cette étude de phase III randomisée menée en ouvert a été réalisée dans 38 hôpitaux français (Groupe Français de Pneumo-Cancérologie) avec inclusion sur la période juillet 2013-juillet 2018 de 164 patients (≥ 18 ans, ECOG 0-2) présentant un cancer bronchique à petites cellules (CBPC) stade IV ou avec récidive locale ayant répondu à une 1re ligne de sel de platine + étoposide mais avec une rechute ou une progression au moins 90 jours après la fin du traitement de 1re ligne. Les patients ont été randomisés (1:1) pour recevoir une combinaison carboplatine + étoposide (6 cycles de carboplatine i.v. ASC 5 mg/mL/min à J1 + étoposide i.v. 100 mg/m2 de J1 à J3) ou du topotécan par voie orale (2,3 mg/m2 de J1 à J5 sur 6 cycles). Le critère principal d’évaluation était la survie sans progression (SSP) analysée en ITT (revue centralisée). Au total, les résultats portent sur 162 patients analysables (81 dans chaque groupe). Avec un suivi médian de 22,7 mois (IQR 20,0-37,3), la SSP médiane est significativement plus longue dans le bras combinaison en comparaison au bras topotécan seul : 4,7 mois (IC95 : 3,9-5,5) versus 2,7 mois (IC95 : 2,3-3,2) (HR = 0,57 ; IC95 : 0,41-0,73 ; p = 0,0041) (figure). Les analyses de sous-groupes confirment ces résultats et en analyse multivariée, seuls le bras de traitement et la radiothérapie cérébrale à visée prophylactique sont significativement associés avec une meilleure SSP.
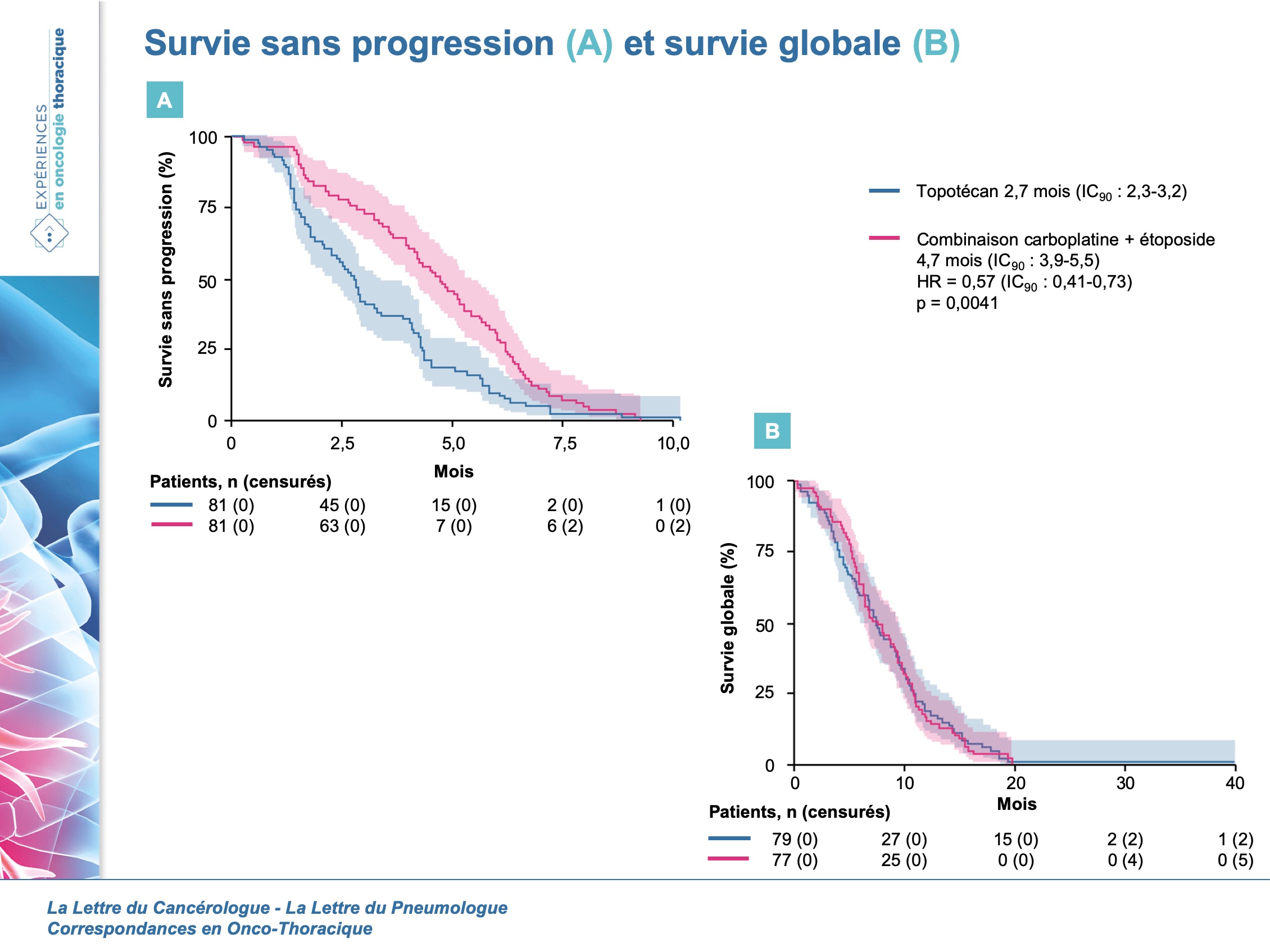
Au moment de l’analyse, la survie globale médiane est comparable entre les deux bras : 7,5 mois (IC95 : 5,4-9,5) dans le bras carboplatine + étoposide versus 7,4 mois (IC95 : 6,0-8,7) dans le bras topotécan (HR = 1,03 ; IC95 : 0,87-1,19 ; p = 0,94). Le taux de réponse objective (RO) est plus élevé dans le bras combinaison : 49 versus 25 % (p = 0,0024) avec une durée médiane de réponse, respectivement de 5,4 et 4,1 mois. Les effets indésirables de grade 3-4 les plus fréquents étaient les neutropénies (22 % dans le bras topotécan versus 14 % dans le bras combinaison), les thrombocytopénies (respectivement 36 versus 31 %), les anémies (21 vs 25 %), les neutropénies fébriles (11 versus 6 %) et les asthénies (10 versus 9 %). Deux décès en rapport avec l’administration du traitement ont été constatés dans le bras topotécan (2 neutropénies fébriles avec sepsis) versus aucun décès en rapport avec l’administration du traitement dans le bras combinaison. Les autres décès survenus étaient en rapport avec la maladie.
Ce que cet article apporte à ma pratique :
- Le rechallenge par carboplatine + étoposide est une option envisageable de 2e ligne dans les rechutes de CBPC ‟sensibles” ;
- Le critère principal (SSP) a été atteint, le taux de RO est supérieur avec un profil de tolérance globalement en faveur de la combinaison.
Références
1. Baize N et al. Carboplatin plus etoposide versus topotecan as second-line treatment for patients with sensitive relapsed small-cell lung cancer: an open-label, multicentre, randomised, phase 3 trial. Lancet Oncol 2020;21:1224-33.
















