Efficacité du lorlatinib chez le patient atteint d’un cancer du poumon ROS-1 positif
Les réarrangements de ROS1 sont identifiés chez environ 1 à 2 % des patients atteints d’un cancer du poumon non à petites cellules (CPNPC) et définissent un sous-ensemble moléculaire distinct de CPNPC présentant une sensibilité à l’inhibition de ROS1. La majorité des patients ROS1-positifs traités par le crizotinib répondent initialement au traitement, mais la plupart d’entre eux récidivent à cause de l’apparition d’un mécanisme de résistance. Le lorlatinib est un inhibiteur tyrosine kinase (ITK) de troisième génération qui cible les récepteurs ALK et ROS1 avec une activité préclinique contre la plupart des mutations de résistance connues des récepteurs ALK et ROS1.
Dans cet article, A. Shaw et al. (1) présentent les résultats d’une étude de phase I et II sur l’activité antitumorale et la sécurité du lorlatinib chez des patients présentant un CPNPC ROS1 positif. Les patients éligibles présentaient un CPNPC métastatique avec un réarrangement ROS1 et un performance status ≤ 2. Les métastases cérébrales (SNC) asymptomatiques ont été admises avec ou sans traitement. Les patients atteints d’une maladie leptoméningée ou d’une méningite carcinomateuse étaient éligibles dans l’étude de phase II si la maladie leptoméningée ou la méningite carcinomateuse était visualisée sur IRM ou si la cytologie initiale du liquide céphalorachidien était positive. Les patients naïfs et les patients déjà traités pour un inhibiteur de la ROS1 étaient éligibles.
Le critère d’évaluation principal était la réponse tumorale objective et la réponse tumorale intracrânienne selon la version 1.1 modifiée de RECIST.
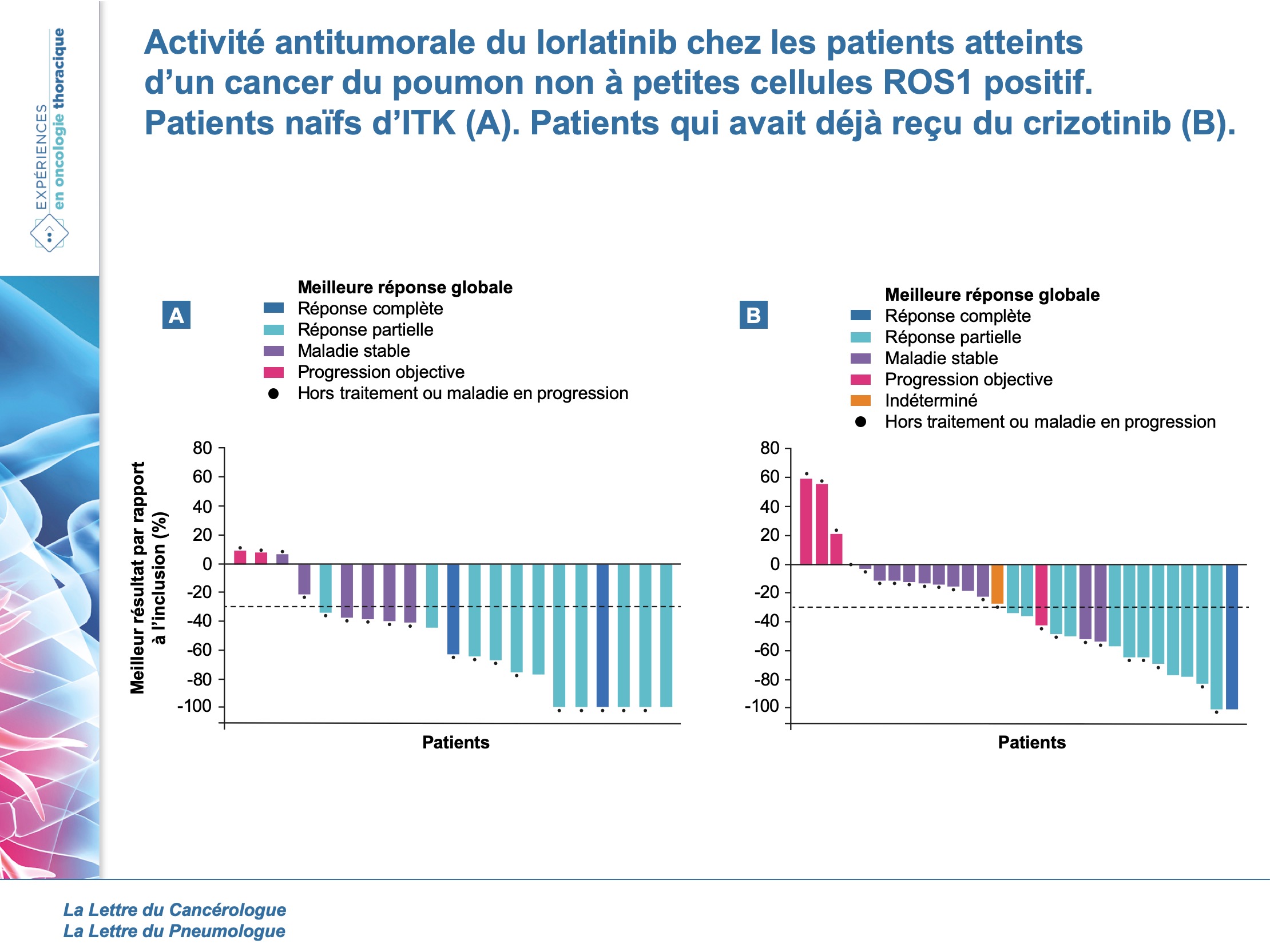
Au total, 69 patients atteints d’un CPNPC ROS1 positif ont été recrutés. 21 (30 %) des 69 patients n’avaient jamais reçu un ITK, 40 (58 %) avaient déjà reçu du crizotinib comme seul ITK et 8 (12 %) avaient déjà reçu un ITK ROS1 (mais pas crizotinib) ou deux ou plusieurs ROS1 ITK. Des métastases du SNC étaient présentes au départ chez 39 (57 %) des 69 patients, dont 19 (49 %) avaient déjà reçu une radiothérapie encéphalique. Parmi les 69 patients atteints d’un CPNPC ROS1 positif, 28 (41 %) avaient une réponse objective. Sur les 21 patients n’ayant jamais reçu un ITK, 13 (62 %) avaient montrés une réponse objective (figure 1A). Des réponses objectives ont été obtenues chez 5 (45 %) des 11 patients ayant des métastases cérébrales au départ. Sur les 40 patients qui avaient reçu du crizotinib comme seul traitement antérieur, des réponses objectives ont été observées chez 14 patients (35 %) (figure 1B). Des réponses ont été observées chez 6 (25 %) des 24 patients présentant des métastases cérébrales au départ. Sur les 24 patients traités par le crizotinib qui présentaient des métastases cérébrales au départ, 12 (50 %) ont obtenu une réponse intracrânienne. Sur les 10 patients traités par crizotinib qui présentaient des métastases mesurables dans le SNC au départ, 5 (50 %) ont présenté une réponse intracrânienne. La durée médiane de la réponse intracrânienne n’a pas été atteinte.
Sur 69 patients traités par le lorlatinib, 66 (96 %) ont présenté au moins un effet indésirable lié au traitement. Les effets indésirables liés au traitement de grade 3-4 les plus fréquents étaient l’hypertriglycéridémie (13 patients) et l’hypercholestérolémie (10 patients). Aucun décès dû à des événements indésirables n’a été observé. Des effets indésirables graves liés au traitement sont survenus chez cinq (7 %) des 69 patients. Des interruptions temporaires de traitement associées à des effets indésirables liés au traitement ont été signalés dans 25 (36 %) des 69 patients et des réductions de dose associées à des effets indésirables liés au traitement ont été signalés chez 17 (25 %) patients.
Le lorlatinib a montré une activité clinique chez les patients atteints d’un CPNPC ROS1 positif, y compris ceux atteints de métastases dans le SNC et ceux ayant déjà reçu du crizotinib. Comme les patients réfractaires au crizotinib ont peu d’options thérapeutiques, le lorlatinib pourrait représenter une importante option thérapeutique.
Ce que cet article apporte à ma pratique :
- La plupart des patients atteints de ROS1 positifs traités par le crizotinib développent une résistance au médicament.
- Le lorlatinib est un inhibiteur tyrosine kinase (ITK) de troisième génération avec une activité préclinique contre la plupart des mutations de résistance connues des récepteurs ALK et ROS1.
- Cette étude de phase I et de phase II visait à évaluer la réponse tumorale objective et la réponse tumorale intracrânienne chez les patients traités par lorlatinib soit en première ligne, soit après progression en cours de crizotinib.
- 62 % des patients ITK naïfs et 35 % des patients ayant déjà reçu du crizotinib comme seul ITK ont démontré une réponse objective.
- Les effets indésirables liés au traitement de grade 3-4 les plus fréquents étaient l’hypertriglycéridémie (19 %) et l’hypercholestérolémie (14 %). Des effets indésirables graves liés au traitement sont survenus chez 7 % des patients.
- Le lorlatinib a montré une activité chez les patients ROS1 positif, y compris ceux atteints de métastases cérébrales et ceux ayant déjà reçu du crizotinib.
À retenir : Le lorlatinib représente un important traitement de deuxième ligne chez les patients ROS1 réfractaires au crizotinib, y compris ceux qui présentent des métastases cérébrales.
Références
1. Shaw AT et al. Lorlatinib in advanced ROS1-positive non-small-cell lung cancer: a multicentre, open-label, single-arm, phase 1–2 trial. Lancet Oncol 2019 ; doi :10.1016/S1470-2045(19)30655-2 [Epub ahead of print].
















