Immunothérapie pour les patients porteurs d’un cancer bronchique avancé avec altérations moléculaires : résultats du registre IMMUNOTARGET
L’immunothétapie se positionne actuellement comme la pierre angulaire du traitement des cancers bronchiques non à petites cellules (CBNPC) localement avancés ou métastatiques avec une amélioration de la survie globale en 1re ligne chez les patients sans addiction oncogénique (1-2).
L’objectif de l’étude de J. Mazières et al. (3) était d’évaluer l’efficacité de l’immunothérapie en monothérapie chez les patients porteurs d’une addiction oncogénique.
Un large réseau international d’oncologues thoraciques de 24 centres répartis dans 10 pays différents ont été sollicités. Pour être inclus, les patients devaient être porteurs d’un CBNPC, traités par un anti-PD1 ou PD-L1 en monothérapie, avec au moins une des altérations moléculaires suivantes : mutation d’EGFR (exon 18-21), d’HER2 (exon 20), de KRAS, de BRAF (exon 15), mutation de l’exon 14 ou amplification de MET, réarrangement d’ALK, de ROS1 ou de RET. Le statut PD-L1 était évalué dans chaque centre, de même que le statut mutationnel, par séquençage direct ou NGS.
L’objectif principal était la survie sans progression (SSP) dans pour chaque addiction oncogénique. Les objectifs secondaires étaient le taux de réponse et la survie globale (SG).
Ainsi, 551 patients ont été inclus de façon rétrospective : 271 KRAS, 125 EGFR, 43 BRAF (dont 18 non V600E), 36 MET (23 mutations de l’exon 14 et 13 amplifications), 29 HER2, 23 ALK, 16 RET et 7 ROS1. L’âge médian était de 60 ans, avec autant d’hommes que de femmes, 28 % de patients non fumeurs et le PS à l’introduction de l’immunothérapie était majoritairement à 1 (64 %). Les patients ont essentiellement été traités par nivolumab, en seconde ligne ou au-delà, avec un nombre moyen de 5 cycles.
Le taux de PD-L1, disponible pour 39 % des patients, était < 1 % pour 33,2 % des patients et ≥ 50 % pour 33,9 %. Certaines altérations moléculaires comme MET, BRAF et ROS1 étaient associées à des taux de PD-L1 élevés.
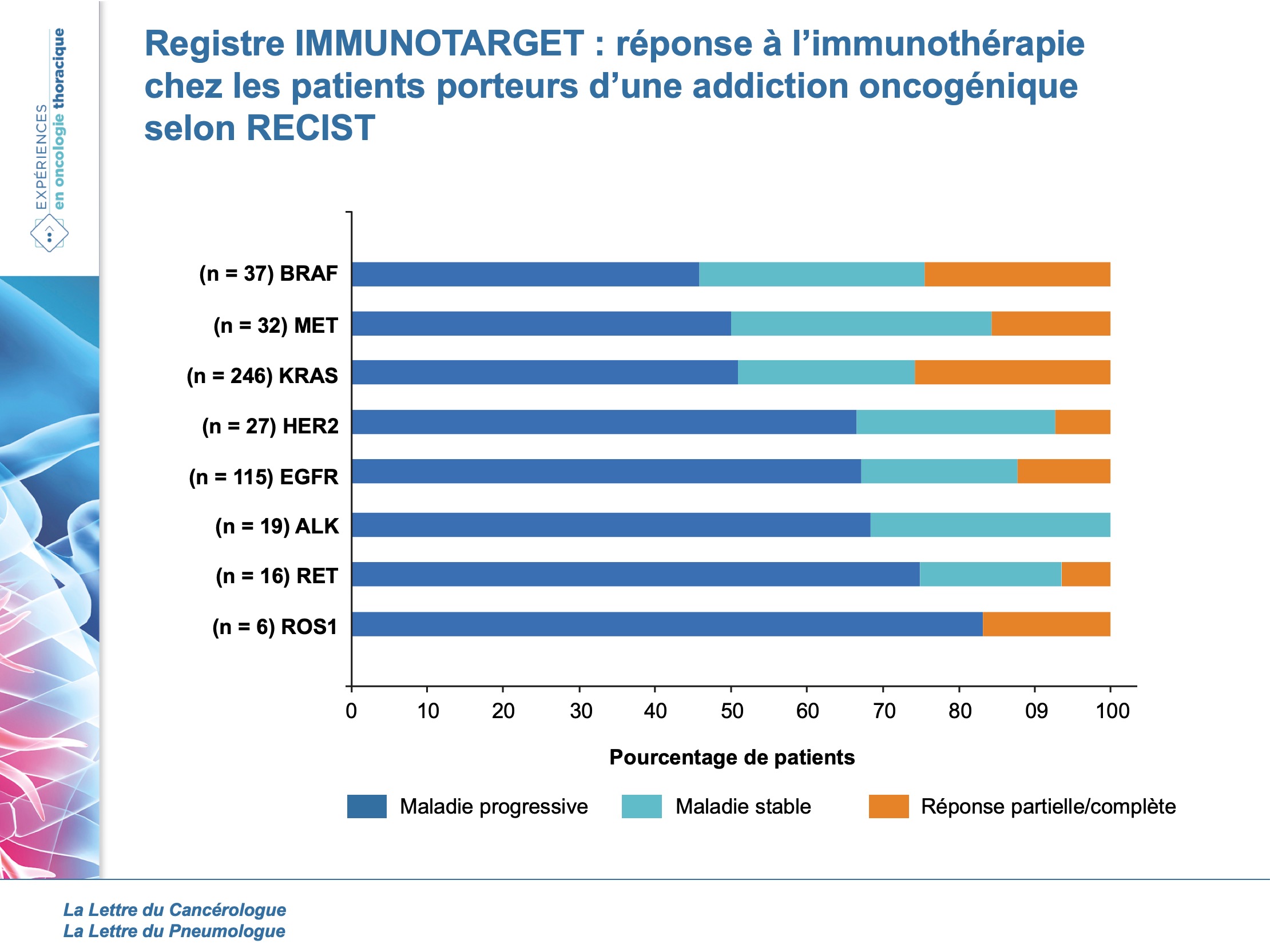
Le taux de réponse moyen était de 19 % avec une médiane de SSP de 2,8 mois dans l’ensemble de la cohorte et une survie globale de 13,3 mois à partir de l’introduction de l’immunothérapie. En excluant les patients KRAS, les taux de réponse étaient 12,7 % et la médiane de SSP de 2,4 mois avec, de façon notable, aucune réponse observée chez les patients ALK (figure).
En analyse de sous-groupes, le taux de PD-L1 semblait être significativement associé à une amélioration de la SSP chez les patients mutés KRAS et de façon intéressante également chez les patients mutés EGFR. Chez les patients BRAF, 2 facteurs impactaient la SSP : le statut tabagique avec une amélioration significative de la SSP chez les patients fumeurs, et le sous-type de mutations (BRAF V600E versus non V600E) avec une médiane de SSP de 1,8 mois versus 4,1 mois, respectivement (p = 0,2). Chez les patients mutés HER2, on retrouvait également une amélioration significative de la SSP chez les fumeurs.
La tolérance a pu être évaluée sur 83 % des patients, avec parmi eux 11 % d’effets secondaires grade 3 à 5 dont un décès lié à une atteinte endocrinienne. 13 cas de pneumopathie grade 3-4 ont été rapportés.
L’immunothérapie chez les patients porteurs d’une addiction oncogénique hors KRAS semble avoir une efficacité inférieure à celle de la population sans addiction oncogénique. Certains sous-groupes de patients semblent tout de même en bénéficier mais aucun marqueur critère clinique ou biologique ne permet de les identifier. L’immunothérapie en monothérapie peut s’inscrire comme une option à épuisement des thérapies ciblées et de la chimiothérapie. L’association de l’immunothérapie à la chimiothérapie plus ou moins aux antiangiogéniques à progression après thérapies ciblées, comme dans l’essai IMPOWER 150 (4), pourrait également être une option de traitement intéressante et plusieurs essais sont actuellement en cours pour répondre à cette question.
Ce que cet article apporte à ma pratique :
- L’immunothérapie en monothérapie doit être envisagée à épuisement des traitements par ITK et chimiothérapie chez les patients avec une addiction oncogénique hors KRAS.
- Certains sous-groupes pourraient bénéficier de l’immunothérapie en fonction du statut tabagique, du taux d’expression de PD-L1 ou du type de mutations.
- Pas de signal de surtoxicité, notamment au niveau pulmonaire.
















