Osimertinib en adjuvant : résultats de l’essai ADAURA
La chimiothérapie adjuvante est le standard de traitement chez les patients opérés d’un cancer bronchique non à petites cellules de stade IB à IIIA et a permis d’améliorer la survie globale de 5 % à 5 ans (1). Plusieurs essais ont évalué l’intérêt des ITK de l’EGFR en adjuvant chez les patients mutés EGFR opérés, sans mettre en évidence de bénéfice de survie globale (2, 3).
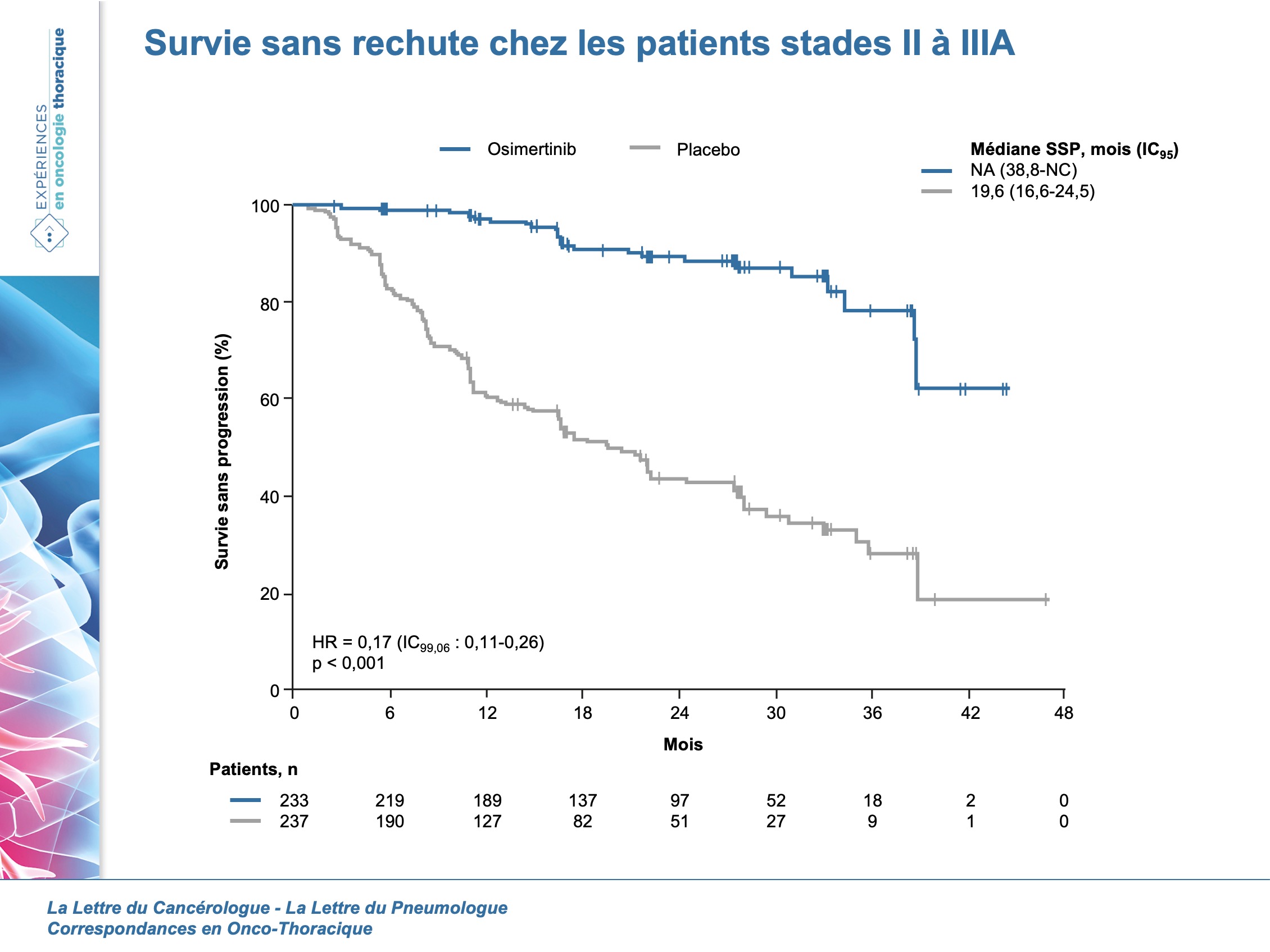
L’essai ADAURA (4) a évalué l’impact sur la survie d’un traitemant adjuvant par osimertinib pendant 3 ans, versus placebo, chez des patients porteurs d’un CBNPC avec mutation activatrice commune (del19, L858R) de l’EGFR, de stade IB à IIIA opérés, en résection complète après chimiothérapie adjuvante ou non, au choix de l’investigateur. L’objectif principal était la survie sans rechute chez les patients stades II à IIIA. Cette analyse intermédiaire n’était pas programmée et a été réalisée suite à la demande du comité de relecture indépendant 2 ans plus tôt (156 événements au lieu des 247 programmés).
682 patients ont été randomisés en 1:1 entre les 2 groupes avec une répartition homogène entre les stades. 55 % ont reçu de la chimiothérapie adjuvante.
Avec un délai médian de suivi de 22,1 (osimertinib) et 14.9 mois (placebo) respectivement, la réduction du risque de rechute était de 83 % chez les patients dans le bras osimertinib (HR = 0,17) et un bénéfice significatif quel que soit le stade (HR = 0,50 ; 0,17 ; 0,12 pour les stades IB, II et IIIA, respectivement) ou le traitement adjuvant par chimiothérapie.
Les premières données sur les sites de rechute ont également été présentées. Elles sont à interpréter de façon prudente compte tenu du manque de maturité des résultats. La proportion de rechutes métastatiques à distance semble plus élevée chez les patients du groupe placebo, avec un effet protecteur de l’osimertinib sur les rechutes cérébrales (HR = 0,18). En terme de toxicité, des effets secondaires de grade 3 ou plus, ont été rapportés chez 20 % des patients du bras osimertinib contre 13 % du bras placebo, sans événement fatal dans le bras osimertinib.
L’amélioration de la survie sans rechute avec l’osimertinib en adjuvant pendant 3 ans est spectaculaire avec des données préliminaires montrant une limitation du risque de rechute cérébrale, ce qui semble capital d’un point de vue clinique pour les patients. Les données de SG ne seront pas disponible tout de suite mais sont très attendues car, jusque-là, les études avec les ITK de 1re génération n’ont pas montré de bénéfice. Cependant, un bénéfice de SG est-il indispensable à la prescription d’un traitement adjuvant avec une tolérance satisfaisante sans risque de surmortalité ? La survie sans rechute et sans métastases cérébrales ne peut-elle suffire ? Des biomarqueurs permettraient-ils de mieux évaluer les patients bénéficiant de ce traitement ? De nombreuses questions restent en suspend en attendant des résultats plus matures de l’essai ADAURA.
Ce que cet article apporte à ma pratique :
- Bénéfice majeur en survie sans rechute de l’osimertinib en adjuvant chez les patients EGFR mutés opérés en résection complète avec effet protecteur cérébral.
- Pas encore d’AMM dans cette indication.
- Si l’osimertinib adjuvant devenait un standard, impact majeur sur le testing moléculaire qui devrait être étendu à tous les stades de CBNPC non épidermoïdes.
Références
1. Pignon JP et al. Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. JCO 2008;26:3552-9.
2. Yue D et al. Erlotinib versus vinorelbine plus cisplatin as adjuvant therapy in Chines patients with stage IIIA EGFR mutation-positive non-small-cell lung cancer (EVAN): a randomised, open-label, phase 2 trial. Lancet Respir Med 2018;6:863-73.
3. WU YL et al. CTONG 1104: adjuvant gefitinib versus chemotherapy for resected N1-N2 NSCLC with EGFR mutation - ,Final overall survival analysis of the randomized phase 3 trial. ASCO 2020; abstr. 9005.
4. Wu YL et al. Osimertinib in resected EGFR-mutated non–small-cell lung cancer. N Engl J Med 2020;383:1711-23.
















