Brolucizumab : durée d’action et résultats anatomiques
L’introduction des anti-VEGF dans le traitement des pathologies rétiniennes a constitué une vraie révolution, ayant pour résultat le changement des paradigmes de traitement des patients atteints, ainsi qu’un meilleur pronostic visuel.
Parmi les anti-VEGF, la molécule la plus récente ayant bénéficié d’une AMM est le brolucizumab, qui a été étudié dans les études HAWK et HARRIER. Il s’agit d’une molécule de petite taille, ce qui permet d’augmenter la concentration de la molécule dans le volume injecté. Les études HAWK et HARRIER ont analysé le brolucizumab (3 et 6 mg) en face à face à l’aflibercept 2 mg, chez des patients atteints de DMLA néovasculaire, le critère principal étant la non-infériorité fonctionnelle. En plus d’avoir prouvé la non-infériorité en termes d’acuité visuelle par rapport à l’aflibercept, ces études ont démontré également une supériorité anatomique du brolucizumab, avec une diminution plus importante de l’épaisseur centrale rétinienne par rapport à l’aflibercept dès les semaines 16 et 48 et maintenue à la semaine 96, avec un assèchement plus important du liquide sous- et intrarétinien dès la semaine 16 et maintenu sur 2 ans. De façon intéressante, plus de 80 % des patients traités par brolucizumab 6 mg en Q12 ont maintenu le régime Q12 après le 1er cycle en Q12 et plus 75 % ont continué sur un régime Q12 au cours de la 2e année (figure).
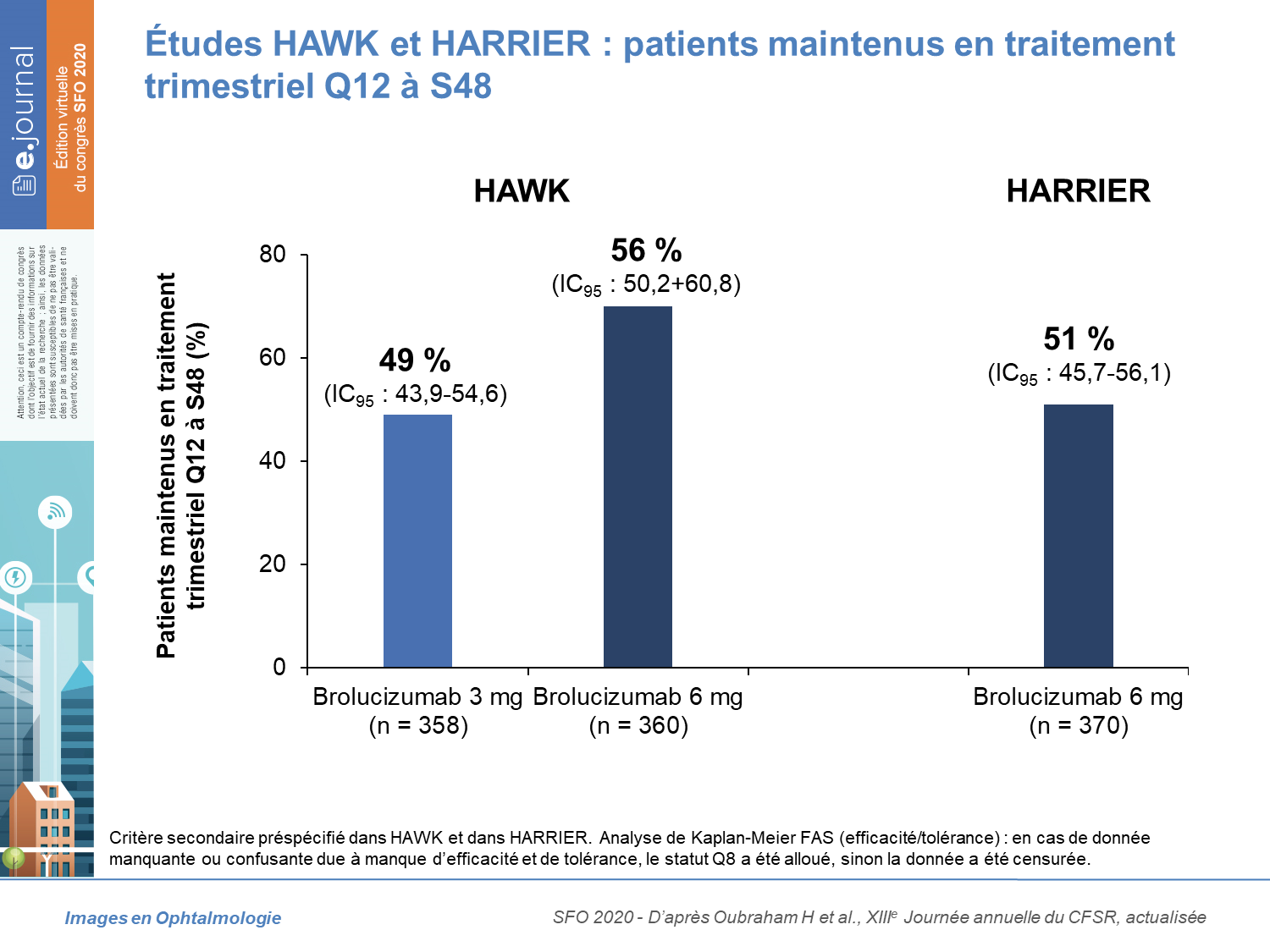
Cependant, dans les études HAWK et HARRIER, puis en surveillance post-marketing dans les pays où il est commercialisé, certains effets indésirables sévères ont été décrits dans de très rares cas, à type d’occlusions vasculaires et d’inflammation, qui justifieront une surveillance plus attentive des patients présentant des facteurs de risque.
Ces résultats montrent que le brolucizumab a une durabilité plus importante, avec la possibilité de prévoir l’intervalle de retraitement dès la 16e semaine et un excellent assèchement du fluide intra- et sous-rétinien.
La durée d’action et les résultats anatomiques du brolucizumab se traduisent, pour les patients, par une plus grande adhésion au traitement, et pour les ophtalmologistes, quand ce produit sera commercialisé en France, par une meilleure planification du suivi de ces patients.








