Efficacité du sécukinumab dans la maladie de Verneuil modérée à sévère : résultats de l’étude de phase III SUNSHINE et SUNRISE
Les études SUNSHINE (NCT03713619) et SUNRISE (NCT03713632) étaient des essais multicentriques de phase III identiques, randomisés, comparées au placebo, évaluant l'efficacité et la tolérance du sécukinumab chez des adultes atteints de la maladie de Verneuil modérée à sévère. Des analyses de l’efficacité primaire du sécukinumab à 16 semaines ont été déjà rapportées.
Il est rapporté dans ce travail les résultats d'efficacité pour les patients traités par SECQ2W ou SECQ4W pendant 52 semaines.
Les patients ont reçu 300 mg de sécukinumab une fois toutes les 2 (SECQ2W) ou 4 (SECQ4W) semaines, ou un placebo entre les semaines 0 à 16. Les patients recevant le placebo ont été re-randomisés pour SECQ2W ou SECQ4W entre les semaines 16 à 52 ; les patients recevant SECQ2W ou SECQ4W sont restés sur le même traitement. La réponse clinique de l'hidradénite suppurée (HiSCR50) était le critère d'évaluation principal.
Dans l'ensemble, 411/541 (76,0 % ; SUNSHINE) et 419/543 (77,2 % ; SUNRISE) des patients ont terminé 52 semaines de traitement. La réponse clinique HiSCR obtenue à la semaine 16 s'est maintenue pendant 52 semaines dans les 2 bras de sécukinumab dans les 2 essais (SUNSHINE : Q2W, 54,8 % [semaine 16, 45,0 %], Q4W, 55,3 % [semaine 16, 41,8 %] ; SUNRISE : Q2W , 63,4 % [semaine 16, 42,3 %], Q4W, 58,6 % [semaine 16, 46,1 %]) (tableau I, figure 1).
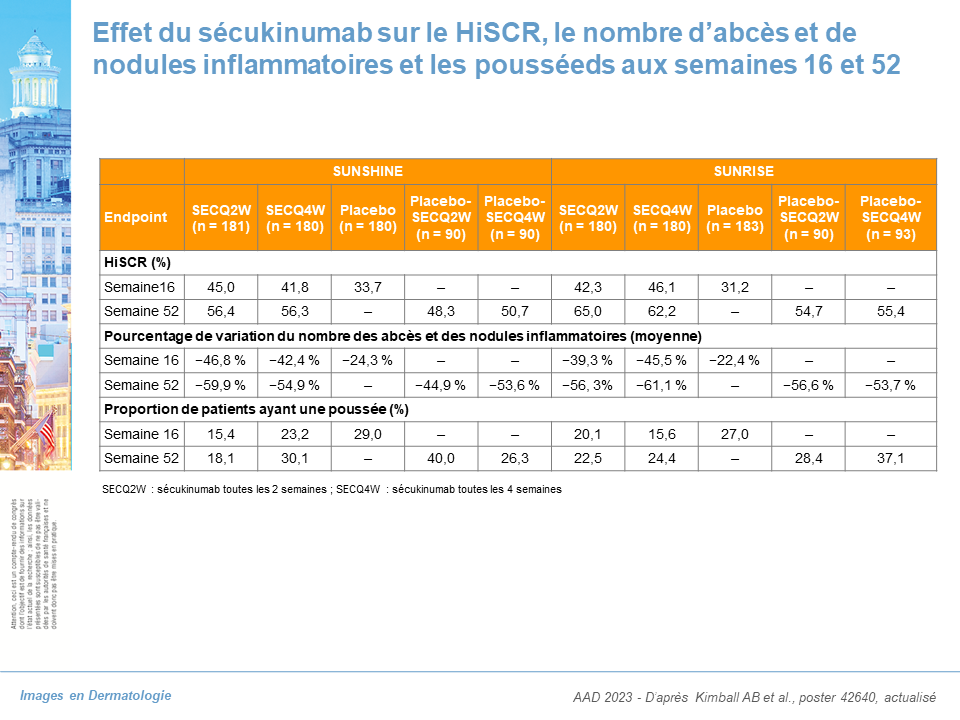
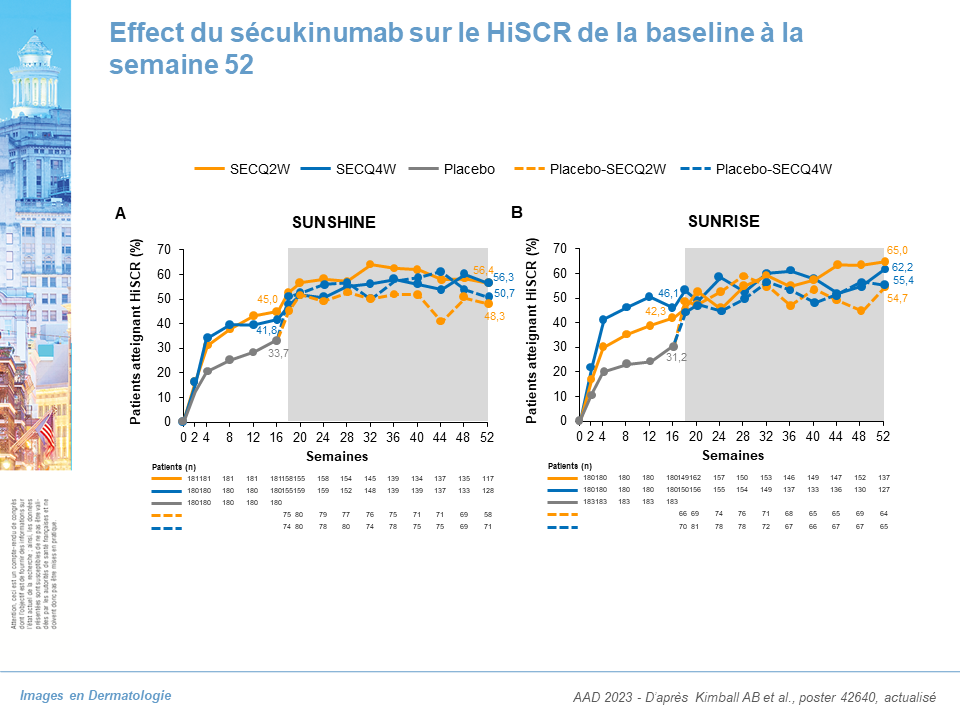
La variation moyenne en pourcentage du nombre d’abcés et de nodules inflammatoires par rapport au départ s'est maintenue avec une tendance à l'amélioration dans les 2 bras sécukinumab jusqu'à la semaine 52 dans SUNSHINE (SECQ2W [−59,9 %], SECQ4W [−54,9 %]) et SUNRISE (SECQ2W [−56,3 %], SECQ4W [−61,1 %]) (tableau I). Une diminution du nombre d’abcès et de nodules inflammatoires a été observée chez les patients passant du placebo à SECQ2W ou SECQ4W à la semaine 16 et les résultats se sont maintenus jusqu'à la semaine 52 (tableau I).
Le taux de poussées est resté faible jusqu'à 52 semaines dans les deux schémas posologiques de sécukinumab dans SUNSHINE (SECQ2W [18,1 %], SECQ4W [30,1 %]) et SUNRISE (SECQ2W [22,5 %], SECQ4W [24,4 %]) (tableau 1). Un meilleur contrôle des poussées a été observé chez les personnes traitées antérieurement par le placebo dans les deux essais de la semaine 16 à la semaine 52 par rapport à celui observé pendant le traitement avec le placebo dans la période de traitement 1 (tableau 1). L'analyse de tolérance à long terme était cohérente avec le profil de tolérance du sécukinumab dans d'autres indications.
L'efficacité du sécukinumab s'est maintenue pendant 52 semaines, montrant une tendance à l'amélioration continue dans le temps, sans qu'aucun nouveau signal de tolérance n'ait été identifié





