DMLA exsudative : les traitements à venir
Le Dr Sylvia Nghiem-Buffet (Paris) a présenté une liste non exhaustive des traitements à venir dans la DMLA exsudative. Nous attendons différents traitements à des échéances variables avec des anti-VEGF à longue durée d'action (brolucizumab, abicipar pégol), d’autres anti-VEGF (conbercept), des traitements combinés (faricimab) et des dispositifs à libération prolongée.
Le brolucizumab (figure 1) est une petite molécule aux propriétés optimisées : solubilité, stabilité et concentration. Les études HAWK et HARRIER ont montré en phase III avec un schéma d’études complexe mais très ingénieux la possibilité de traiter avec des IVT (injections intravitréennes) à 12 semaines plus de la moitié des patients ou à 8 semaines si besoin. Les résultats comparés à ceux de l’aflibercept en Q8 montrent une équivalence en termes d’AV (acuité visuelle) mais une efficacité anatomique accrue de 30 % en moyenne pour le brolucizumab. Ces résultats sont retrouvés à 16, 48 et à 96 semaines. L’AMM est attendue au 1er semestre 2020 avec un remboursement quelques mois plus tard.

L’abicipar pégol ou DARPin est un antagoniste pégylé du VEGF-A (figure 2). Il s’agit de protéines qui miment les anticorps avec une sélectivité et une affinité élevées. Les études SEQUOIA et CEDAR ont montré en phase III une non-infériorité en IVT à 12 semaines comparativement au ranibizumab mensuel. Il existe une petite variation de l’AV dans l’étude CEDAR, mais les résultats “poolés” retrouvent une non-infériorité. L’attention a été attirée sur les inflammations intraoculaires avec une incidence élevée de 15,0 versus 0,3 % pour le ranibizumab. Cette dernière est en cours de correction, comme l’a montré l’étude MAPLE dont les résultats montrent une nette diminution des inflammations intraoculaires à 8,9 % par purification de la molécule. L’AMM déposée en juillet 2019 est attendue pour la fin du 1er trimestre 2020 et le remboursement fin 2021.

Le conbercept (ou KH902) a été présenté (figure 3). Il s’agit d’une molécule chinoise développée pour le marché chinois avec une protéine de fusion recombinante (proche de l’aflibercept). Des études chinoises, notamment PHOENIX, montrent un maintien du gain d’AV en régime fixe Q12 après une phase d’induction. Des études de phase III sont en cours pour une AMM en Europe, en Asie et aux États-Unis, les études PANDA-1 et 2.

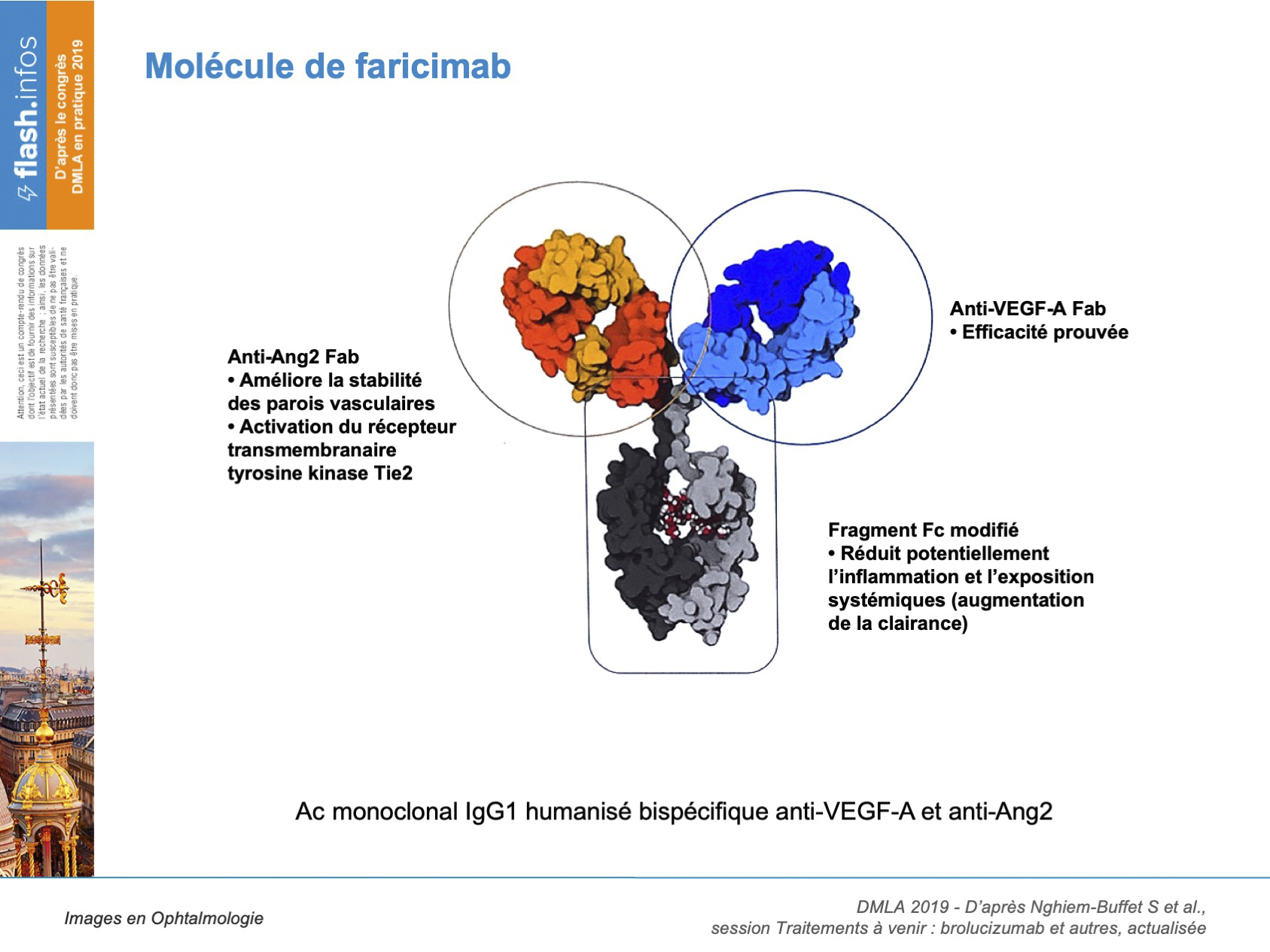
Le faricimab est un anticorps humanisé bispécifique anti-VEGF-A et anti-Ang2 (figure 4). L’étude STAIRWAY a montré en phase II une efficacité et une sécurité en Q12 et Q16 à 52 semaines. Les études de phase III sont en cours, il s’agit de LUCERNE et TENAYA.
Le dispositif à libération prolongée de ranibizumab (ou PDS) une fois implanté chirurgicalement permet d’être rechargé pour libérer progressivement le produit (figure 5). L’étude LADDER en phase II a montré un maintien d’efficacité de plus de 6 mois chez 80 % des patients et un délai médian de recherche à 15 mois. Les résultats ont mis en évidence une non-infériorité par rapport à un traitement mensuel par ranibizumab. L’étude de phase III ARCHWAY est en cours.

En conclusion, le brolucizumab est la molécule la plus proche de la commercialisation. L’abicipar est la deuxième avec un risque inflammatoire hypothétique. L’espoir est principalement d’espacer les injections à 12 semaines. Des questions se posent concernant les intitulés de l’AMM (régime fixe ou “Treat and Extend” ou PRN ?) et le remboursement. Beaucoup d’incertitudes subsistent encore, mais une évolution est attendue dans le traitement de la DMLA exsudative.







