Pas de CAR crash dans le myélome
Les 2 cellules CAR T anti-BCMA les plus avancées dans le traitement du myélome multiple poursuivent leur développement.
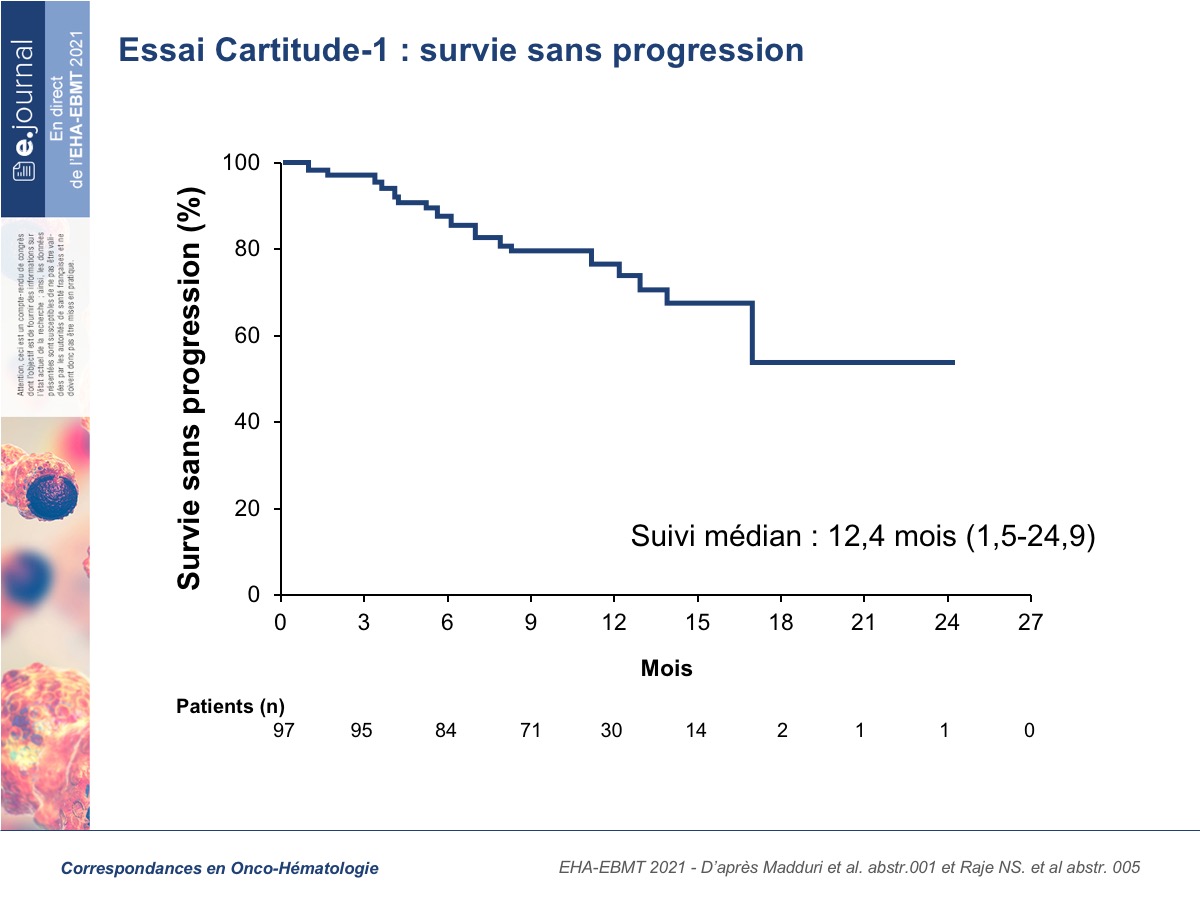
Ciltacabtagene autoleucel (cilta-cel ; JNJ-68284528) est une cellule CAR T anti-BCMA de 2e génération, comprenant un domaine de signalisation CD3ζ, un domaine de costimulation 4-1BB et 2 sites de liaison à BCMA. L’actualisation de l’essai de phase Ib/II rapportée lors de ce congrès portait sur une cohorte de 97 patients, lourdement prétraités (6 lignes antérieures en médiane) et dont 87,6 % étaient triples réfractaires, 42,3 % penta-réfractaires et 99 % réfractaires à la dernière ligne thérapeutique. La tolérance à cilta-cel est acceptable avec un taux de CRS de grade ≥ 3 à 4,1 % et de neurotoxicité de grade ≥ 3 à 9,3 %. 14 patients sont décédés durant l’étude de progression du myélome (n = 5) et de complications reliées et non reliées au cilta-cel chez 6 et 3 patients, respectivement. Le taux de réponse globale est de 97 %, incluant 67 % de réponse complète (RC) et 26 % de très bonne réponse partielle (TBRP). Parmi les 57 patients évaluables pour la maladie résiduelle en NGS, 93 % obtenaient une MRD (minimal residual disease) négative au seuil de 10-5. Avec un recul médian de 12,4 mois, les résultats sont prometteurs puisqu’à 1 an la survie sans progression est de 77 % et la survie globale de 88,5 %. L’essai international de phase III CARTITUDE-4 sera conduit en France en 2021.
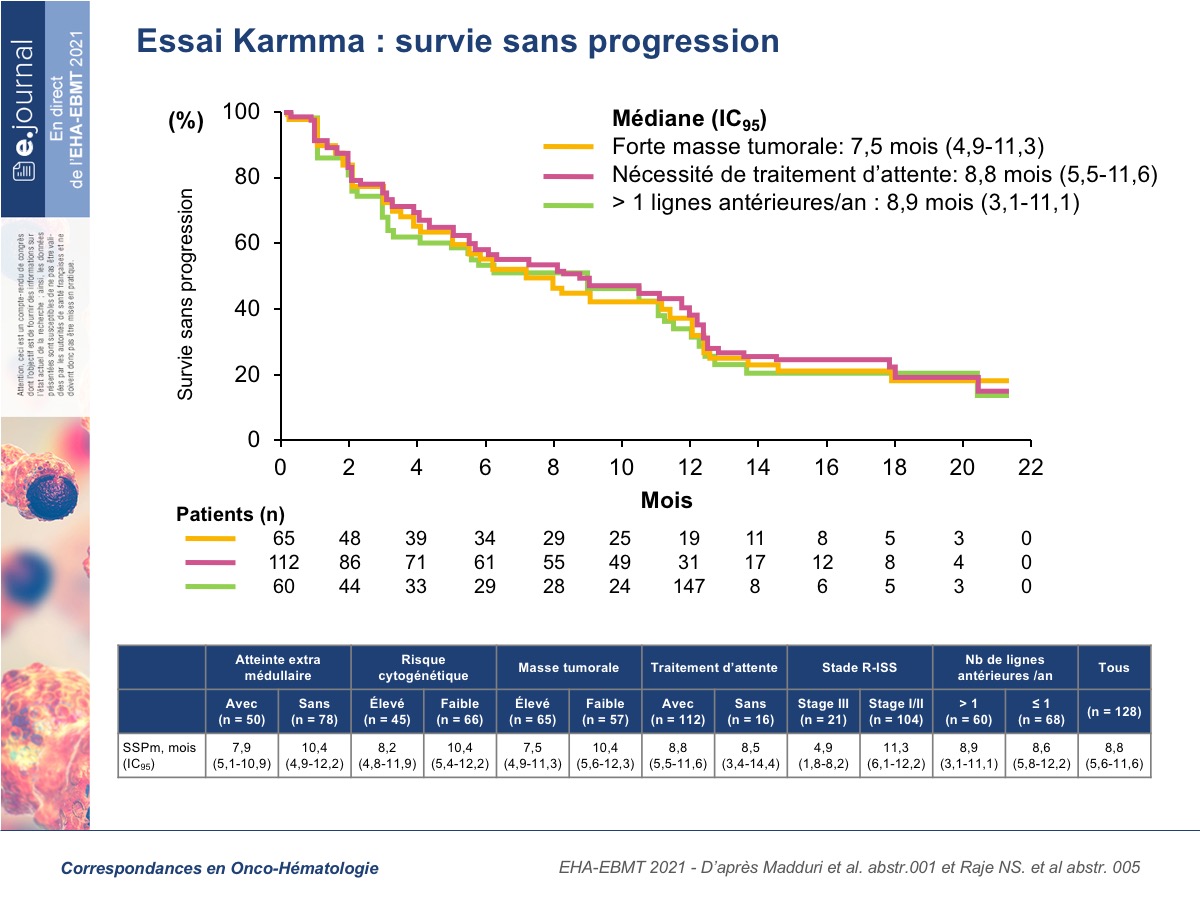
Idecabtagene vicleucel (ide-cel, bb2121) est également une cellule CAR T anti-BCMA CD3ζ / 4-1BB testée chez des patients ayant un myélome progressif. L’essai de phase II KarMMa a inclus 140 patients, dont 128 qui ont été traités par ide-cel (dose, 150-450 × 106 CAR+ T cells). Ils avaient reçu un nombre médian de 6 lignes thérapeutiques antérieures et 84 % étaient triples réfractaires. Le risque cytogénétique était élevé chez 35 % des patients, défini par l’identification d’une del17p, t(4;14) ou t(14;16). Sur l’ensemble de la cohorte, le taux de réponse globale (RC/TBRP/RP) est de 73 %, incluant 33 % de RC. La durée médiane de réponse était de 10,7 mois et la médiane de survie sans progression de 8,8 mois. Le taux de réponse globale était ≥ 65 % dans tous les sous-groupes de haut risque (cytogénétique de haut risque, atteinte extramédullaire, plasmocytose médullaire ≥ 50 %), sauf celui des patients ayant un score R-ISS à III. Un programme d’ATU devrait être activé dans plusieurs centres français dans les prochaines semaines.