ICARIA : synonyme de longévité ?
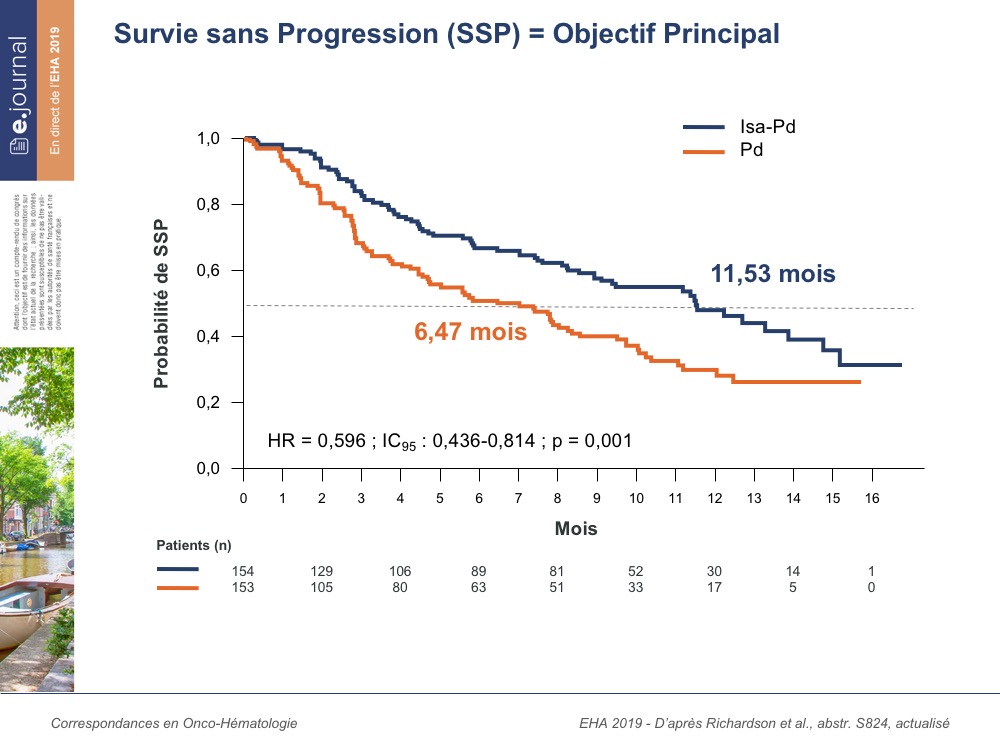
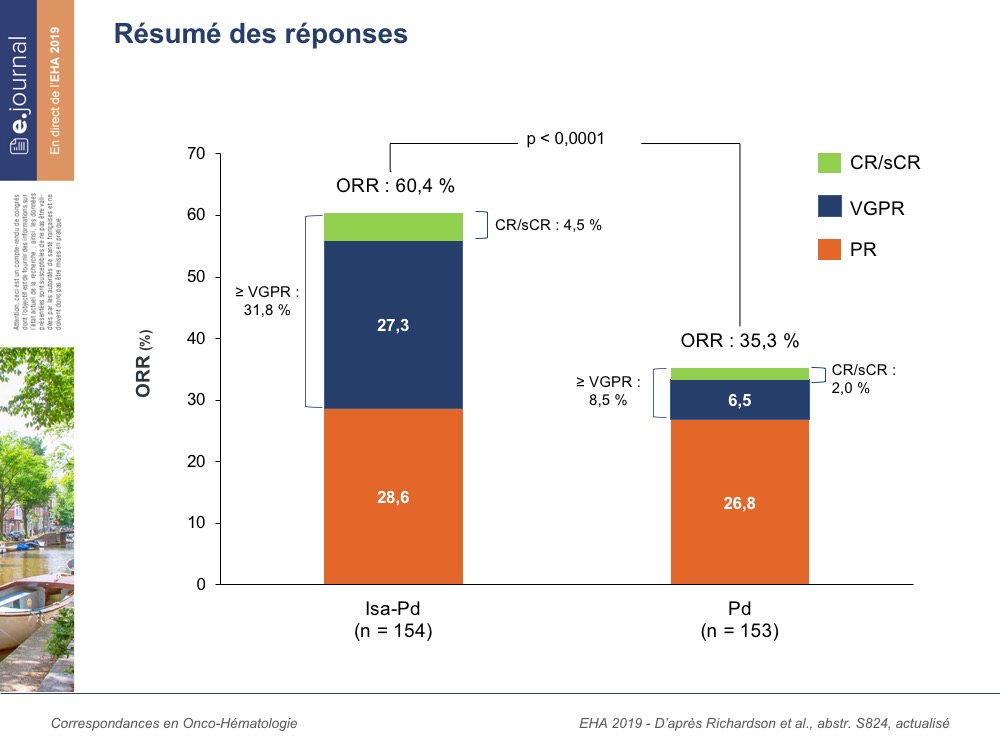
Savez-vous où se trouve Ikaria ? En français cela s’appelle Icarie, appelée également localement Nicaria. C’est une île grecque de la mer Egée orientale, qui tire son nom d’Icare le fils de Dédale dans la mythologie grecque, qui serait tombé dans la mer proche de l’île. Décidément, la mythologie grecque est toujours à l’honneur dans les protocoles du myélome. Une des particularités de l’ile d’Ikaria est la longévité exceptionnelle de sa population où 1 personne sur 3 apparemment atteint les 90 ans. Le choix de ce nom est-il prémonitoire ? En tous cas, ce sont les résultats de l’étude randomisée ICARIA qui ont été rapportés lors de cet EHA 2019. Il s’agit donc d’une étude randomisée de phase III comparant un bras contrôle de type pomalidomide et dexamethasone (Pd) à un bras expérimental incluant isatuximab, pomalidomide et dexamethasone (ISA-Pd) dans le myélome multiple en rechute après au moins 2 lignes incluant lenalidomide et inhibiteurs de protéasome. Comme souvent dans ce type d’étude, l’objectif primaire était la survie sans progression (PFS). L’étude a donc inclus un total de 307 malades ayant une médiane d’âge de 67 ans. 19,5% avaient un haut risque cytogénétique. 153 malades ont été randomisés dans le bras Pd et 154 malades dans le bras ISA-Pd. Le nombre médian de lignes de traitement antérieur était de 3, mais pouvant aller de 2 à 11 dans le bras ISA-Pd. Par définition, 100% des malades avaient reçu un traitement préalable par inhibiteurs de protéasome et par IMID. De manière intéressante 93,5% des patients étaient déjà réfractaires au lenalidomide et 73,4% étaient considérés comme doubles réfractaires. L’étude a atteint son objectif primaire puisque la PFS dans le bras ISA-Pd était de 11,5 mois versus 6,4 mois dans le bras Pd avec un hasard ration à 0,59 (p=0.001). Quand on regarde les différents sous-groupes en fonction de la PFS, on constate que ce bénéfice en termes, de PFS est consistant à travers tous les sous-groupes analysés. En terme de réponse, 31,8% des patients ont atteint une réponse supérieure ou égale à VGPR dans le bras ISA-Pd versus 8,5% dans le bras Pd. Pour ce qui est de la survie globale (OS), et avec un suivi relativement court, nous sommes à 72% à 12 mois dans le bras ISA-Pd, et 63% dans le bras Pd. Le temps jusqu’à un nouveau traitement (TNT), est de 9,1 mois dans le bras Pd et, était non- atteint dans le bras ISA-Pd. De manière intéressante, on constate que plus de 50% des patients dans le bras Pd, qui ont progressé, ont pu recevoir un autre anticorps monoclonal, soit le daratumumab. Côté sécurité, on ne retrouve pas d’effets secondaires majeurs ayant pu entrainer une mortalité excessive ou un arrêt du traitement. Les réactions liées à l’injection de l’isatuximab ont été de l’ordre de 38% et surtout observés lors de la 1ere injection. L’autre élément intéressant est celui d’une qualité de vie maintenue toute à fait comparable entre les deux bras de l’étude.
Au total, cette étude randomisée de phase III, démontre qu’un nouvel anticorps monoclonal anti-CD38, l’isatuximab, est un acteur important dans le traitement du myélome en rechute. Cette étude est la première à démontrer la supériorité d’un anticorps anti-CD38 avec la classique combinaison pomalidomide/dexamethasone. On ne peut que saluer l’arrivée d’un nouvel anticorps monoclonal anti-CD38 car cette classe de médicaments joue un rôle essentiel dans cette pathologie et il est vraisemblable que l’ensemble des différentes lignes de traitement du myélome inclura, à un moment ou un autre, un anticorps anti-CD38.