Voilà le nouvel outsider dans le myélome
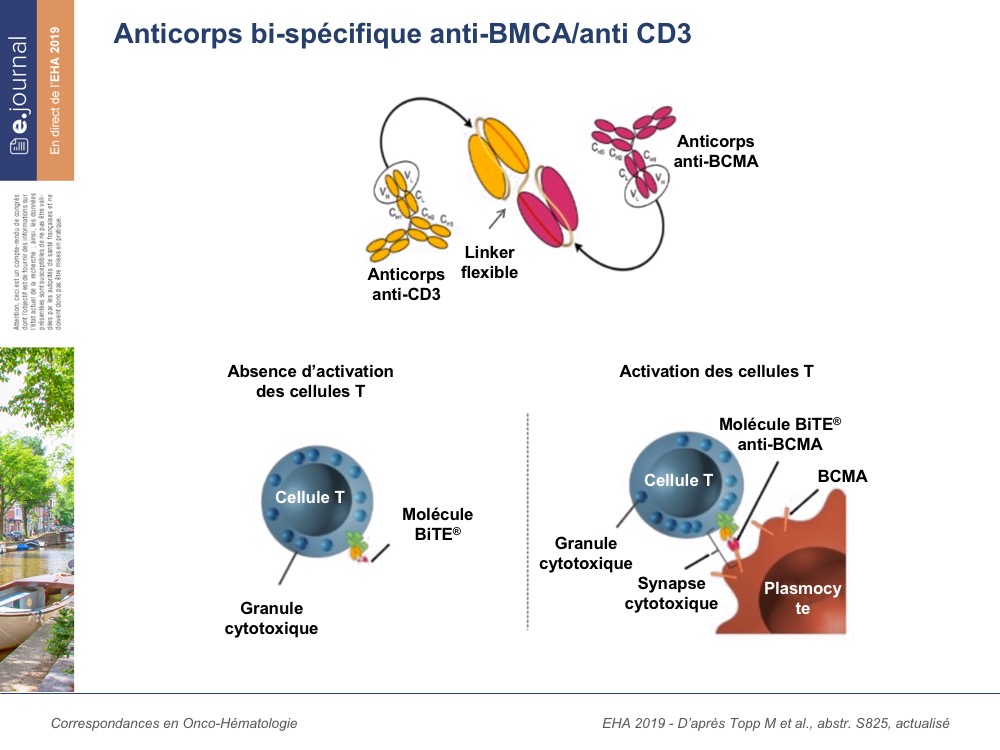
Nous savions déjà que les anticorps monoclonaux anti-CD38, que ce soit le daratumumab ou l’isatuximab, étaient les grands champions du traitement du myélome ces derniers temps. Et voilà qu’un anticorps bispécifique (technologie BITE), l’AMG 420, entre en scène grâce à une phase I d’escalade de doses, rapportée par l’équipe de Würzburg en Allemagne lors de cet EHA 2019. Les anticorps bispécifiques sont déjà connus en hématologie, notamment le blinatumumab qui a son autorisation dans la leucémie aiguë lymphoblastique. Ici, il s’agit d’un anticorps bispécifique dirigé contre l’antigène BCMA, qui est bien exprimé sur les cellules plasmocytaires du myélome. L’étude en question est une étude de phase I d’escalade de doses dite « First In Human » où l’AMG 420 est administré jusqu’à 10 cycles. L’objectif primaire est de déterminer la dose maximale tolérée (MTD), ainsi que la toxicité. Un total de 42 malades a été inclus avec un âge médian de 65 ans (allant de 39 à 79 ans). La durée médiane d’évolution de la maladie avant traitement était de 5,2 années (allant de 1,3 à 20 ans). Les malades ont reçu en médiane 4 lignes de traitement (allant 2 à 13 lignes). 26% avaient déjà reçu le daratumumab et 86% avaient reçu au moins une autogreffe de cellules souches hématopoïétiques. Plus de la moitié des malades était réfractaire aux IMID, ou encore aux inhibiteurs du protéasome. Plusieurs groupes et plusieurs doses ont été analysés et il s’avère que la posologie de 400 µg par jour est celle qui doit être retenue dans la mesure où plusieurs toxicités limitantes ont été observées à la posologie de 800 µg par jour, notamment des cas de syndromes de relargages cytokiniques (CRS). Par ailleurs, il a été observé quelques cas d’infections sérieuses, notamment pulmonaires, mais aussi des réactivations virales avec hépatites fulminantes. Il y a eu aussi deux cas de neuropathies périphériques, et les deux cas ont été considérés comme des toxicités limitantes. Ces deux cas de polyneuropathies périphériques se sont améliorés sous immunoglobulines polyvalentes et corticoïdes. La pharmacocinétique de l’anticorps a été analysée et, en moyenne, les concentrations de l’AMG 420 sont dose-dépendante. Néanmoins, il n’a pas été observé d’anticorps anti-AMG 420 à la posologie de 800 µg par jour. Sur 13 patients qui ont été analysés, on observe 6 rémissions complètes stringentes, 3 rémissions complètes, 2 VGPR et 2 PR. La durée médiane pour obtenir la réponse était d’un mois, et 11 des 13 patients ont répondu au cours du 1er cycle. Les réponses étaient relativement durables pour une médiane de 8,4 mois avec des limites allant de 2,5 à 15,5 mois. Cinq malades répondeurs ont pu obtenir une maladie résiduelle négative. La durée de la négativité de la maladie résiduelle était en médiane de 9,6 mois.
En conclusion, cette étude de phase I, première chez l’homme, de l’anticorps bispécifique AMG 420 établit que 400 µg par jour est la dose tolérée maximum et permet un taux de réponse remarquable de 70%, y compris l’obtention de maladie résiduelle négative. Ces résultats sont très encourageants et d’autres études sont en cours. Même si ses modalités d’administration sont contraignantes en raison de sa demi-vie courte, il est fort probable que, dans les années à venir, on entendra beaucoup parler de l’AMG 420 seul, ou en combinaison, aussi bien en rechute, qu’en première ligne, notamment chez les malades de haut risque.