Asciminib : un as pour les patients intolérants à 2 ITK
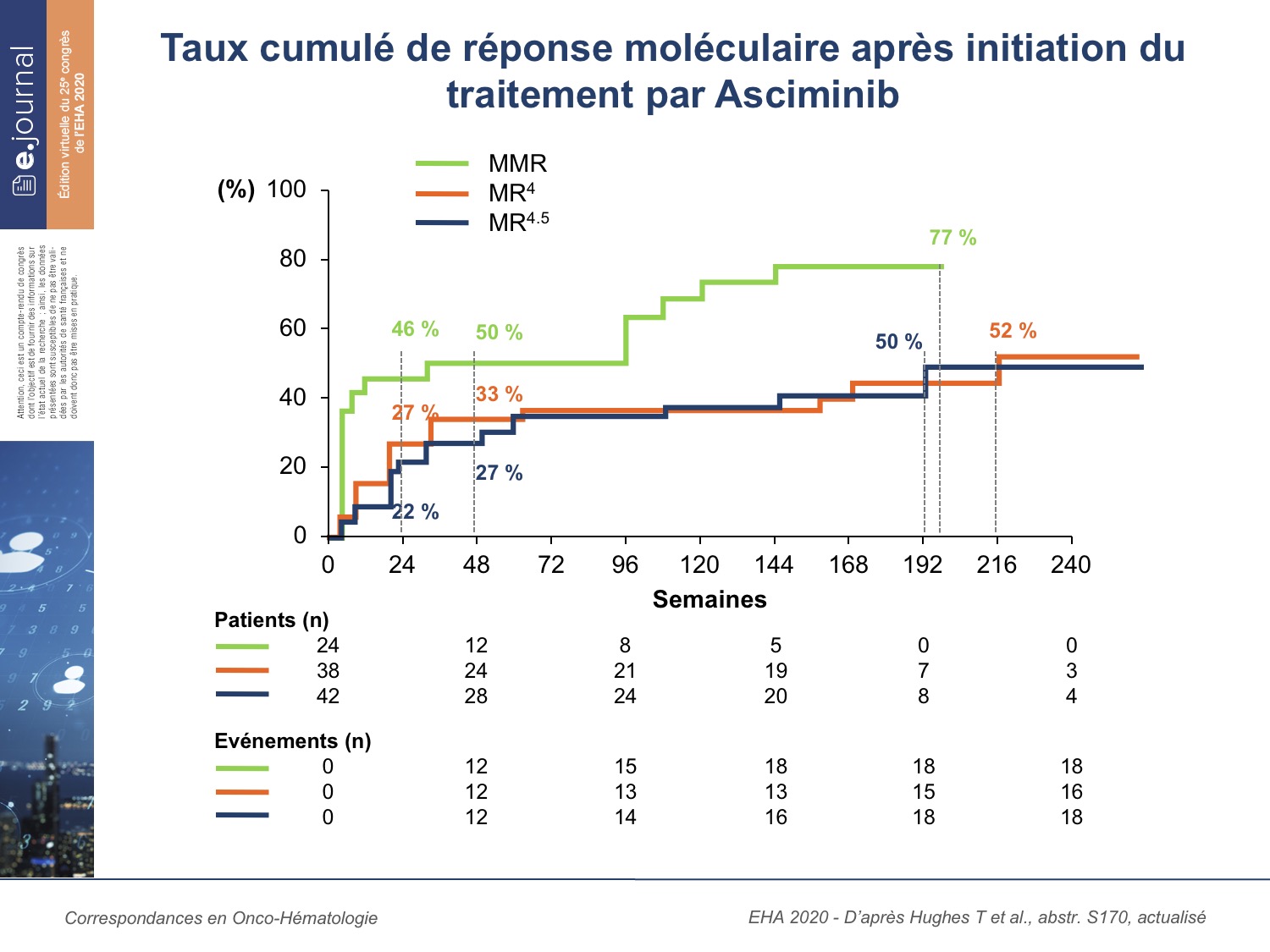
L’asciminib (As) ou ABL001 est un inhibiteur allostérique puissant de BCR-ABL1, dont le mécanisme d’action distinct de celui des Inhibiteurs de tyrosine Kinase (ITK) ATP-compétitifs explique l’excellente tolérance liée à sa spécificité exclusive pour cette kinase. La population étudiée ici, une cohorte de l’essai de phase 1, représente une situation particulière de LMC en phase chronique, moins avancée que dans les précédents rapports d’efficacité/tolérance, d’intérêt clinique quotidien. Il s’agit en effet de patients répondeurs aux ITK classiques, mais de manière insuffisante, soit une majorité de patients intolérants à ≥ 2 ITK. Les critères d’inclusion supposaient en effet un taux de BCR-ABL1IS détectable mais ≤ 1 % et une absence de T315I. Les ITK précédents avaient été arrêtés pour intolérance dans 77 % des cas (isolée dans 27 % des cas, associée à une résistance dans 50 %). La dose d’As initiale était de 40 à 400 mg/j (9 paliers de dose), la durée moyenne d’exposition de 167 semaines (2-271). L’incidence des évènements indésirables (EI) de grade 3-4 était de 33 %, entraînant l’arrêt d’As chez 6 % des patients seulement, alors que plus de la moitié étaient au moins en 4ème ligne d’ITK. Les EI les plus fréquents étaient les hyperlipasémies, comme attendu (27 %), avec 8 % de pancréatites, et les HTA (12,5 %). Une majorité de patients sans Réponse Moléculaire Majeure (RMM de type RM4 ou RM4.5) à l’inclusion, a acquis ce niveau de réponse (figure). La RMM a été obtenue en moyenne en 30 jours, et se maintient à ≥ 2 ans ; les RM4 et RM4.5 se maintiennent chez plus de la moitié des patients. Finalement, 42 patients (87,5 %) sont toujours traités par As et 36 (75 %) sont au moins en RMM à la date d’analyse. L’As permet ainsi l’amélioration d’une réponse aux ITK, antérieurement limitée par une intolérance à l’ITK, et pourrait conduire dans ce contexte à une rémission sans traitement. Au vu d’une comparaison favorable de ces résultats avec ceux de l’essai ENESTcmr basé sur le nilotinib, cet objectif fait l’objet d’un essai de conception voisine, AsForMore.