Mutation TP53 : son mauvais pronostic challengé par l’APR-246 associé à l’azacitidine dans les syndromes myélodysplasiques de haut risque et les leucémies aiguës myéloïdes
La présence d’une mutation TP53 (TP53m) dans les syndromes myélodysplasqiues (SMD) et les leucémies aiguës myéloïdes (LAM) constitue un facteur de très mauvais pronostic avec une survie globale (SG) d’environ 8 mois quel que soit le traitement (Tt) reçu. APR-246 entraîne une re-conformation de p53 avec une réactivation des fonctions préapoptotiques et d’arrêt du cycle cellulaire.
Th. Cluzeau et coll. présentent les résultats de l’étude de phase 2 coordonnée par le Groupe Francophone des Myélodysplasies, avec l’association azacitidine (AZA) et APR-246 dans les SMD et les LAM avec TP53m, naïfs de Tt par hypométhylants et allogreffe.
La réponse, en intention de traitement (ITT), est l’objectif principal. L’analyse a été faite sur toute la population de patients (pts) et celle évaluable après 3 cycles (avec analyse sanguine et médullaire).
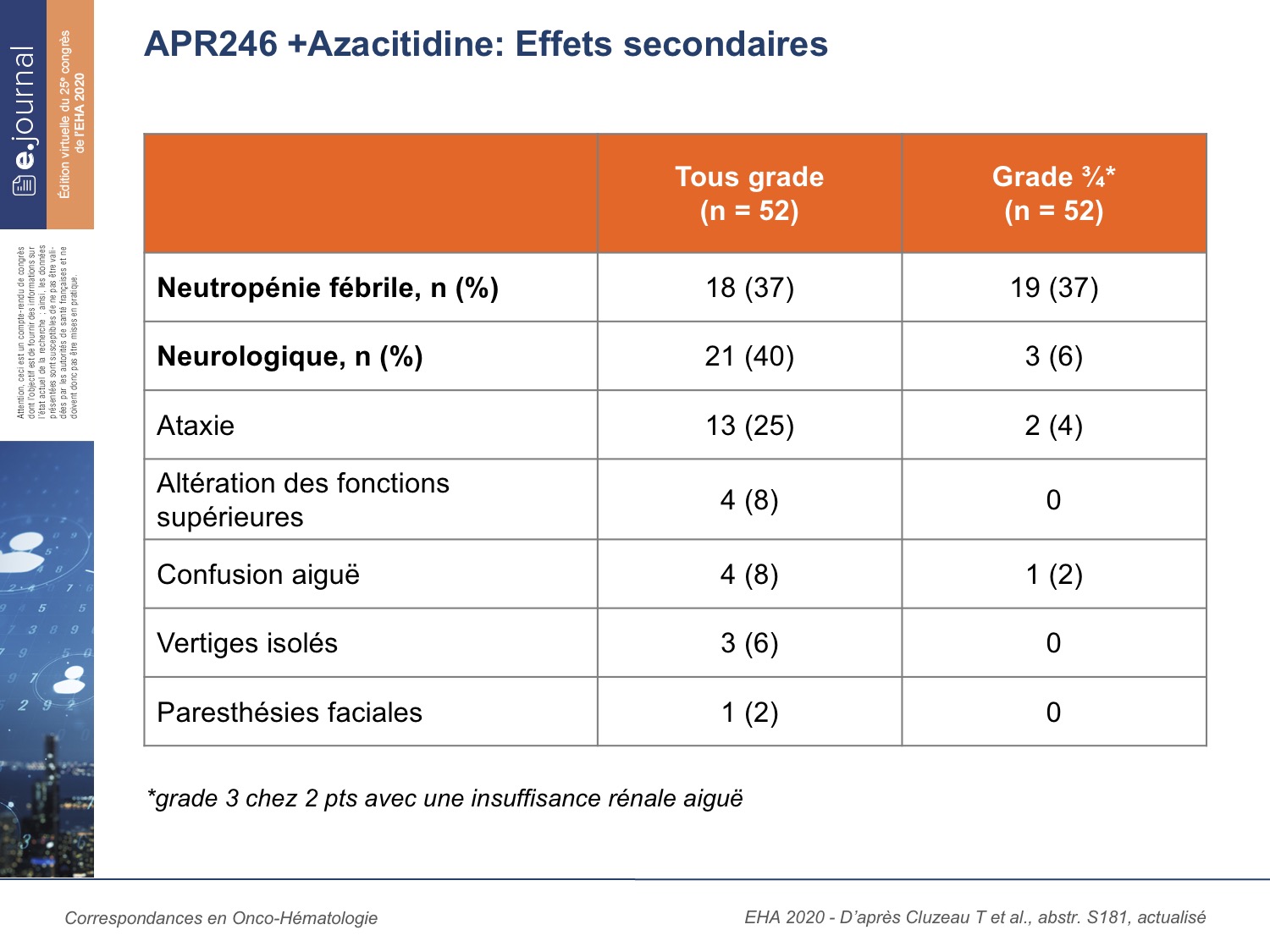
52 pts ont été inclus avec un âge médian de 74 ans (44-87) ; 34 SMD et 18 LAM. 88 % des SMD et 94 % des LAM avaient une cytogénétique de mauvais pronostic ; 87 % avec un caryotype complexe. Les effets indésirables ont été observés chez > 20 % de pts avec, en particulier, une toxicité neurologique chez 21 pts (40 %) corrélés avec une altération de la fonction rénale à l’initiation du traitement (p < 0,01) et à l’âge avancé (p = 0,05), tous réversibles à l’arrêt de l’APR-246 (figure 1).
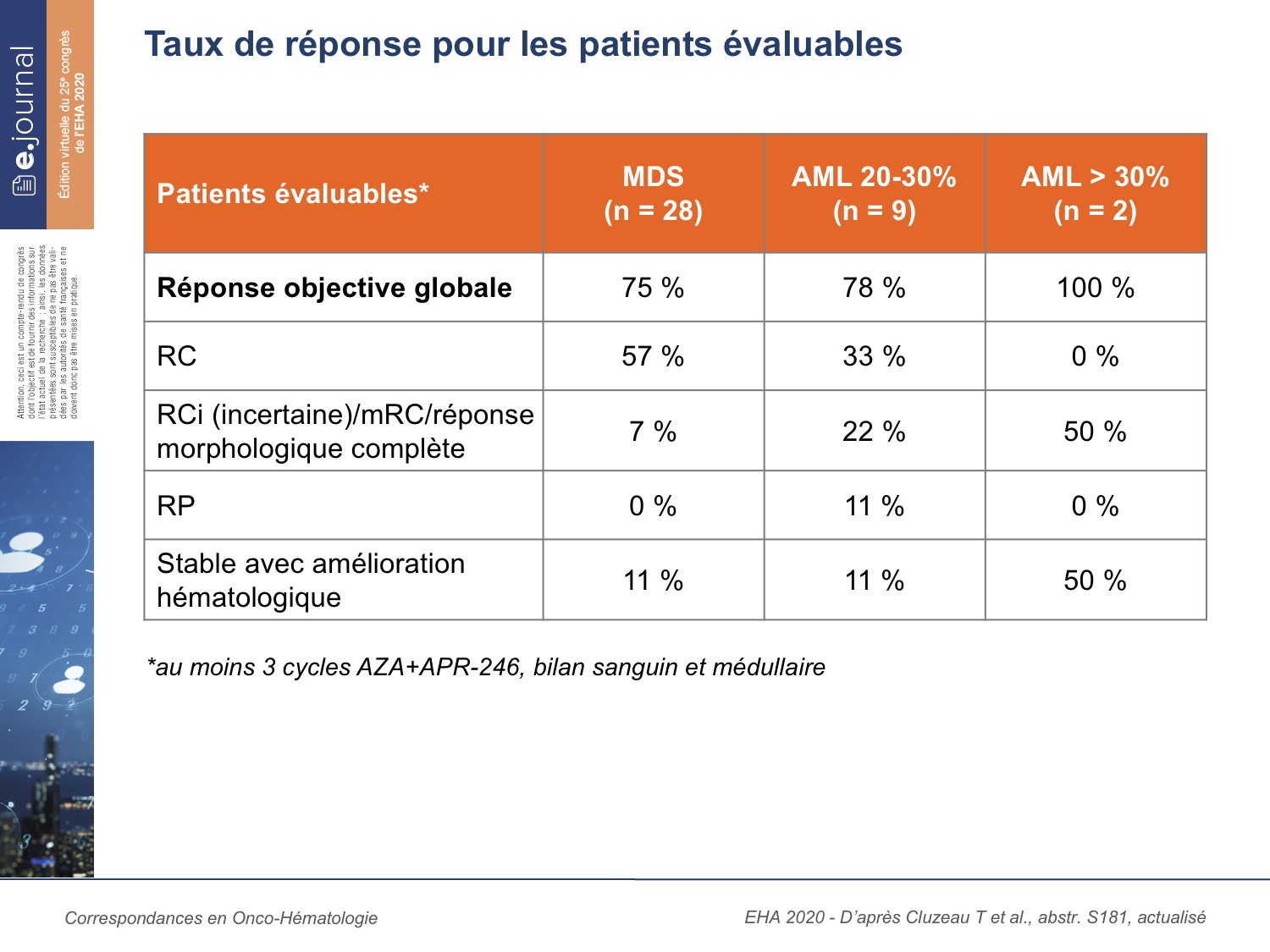
Au moment de l’analyse, 39 pts avaient reçu 3 cycles et étaient évaluables (figure 2). Le taux de réponse globale est de 77 % dont 49% de RC. Pour les pts avec un SMD les taux de réponse global et de RC sont, respectivement, de 75 % de 57 % et pour les LAM, de 78 et 33 %. La médiane de SG est de 12,1 mois et de 13,7 mois pour les pts ayant reçu au moins 3 cycles.
Ces résultats très prometteurs sont toutefois sous-tendus par une toxicité non négligeable imposant un suivi très étroit de ces patients pour la plupart âgés. Une étude de phase 3 randomisée, AZA vs AZA+APR-246 est en cours d’initiation.