Nivolumab + ipilimumab : enfin un marqueur prédictif de réponse ?
La combinaison des inhibiteurs de point de contrôle immunitaire nivolumab (NIVO) + ipilimumab (IPI) a démontré un bénéfice clinique durable à long terme par rapport à la chimiothérapie (CT) dans le cancer bronchique non à petites cellules (CBNPC) métastatique.
L’association NIVO + IPI, en association à 2 cycles de CT à base de sels de platine, constitue une alternative au traitement par pembrolizumab (en monothérapie uniquement si PD-L1 ≥ 50 % ou associé à une CT quelle que soit l’expression de PD-L1) en tant que traitement de 1re ligne des patients adultes atteints d’un CBNPC métastatique, dont les tumeurs n’ont pas la mutation sensibilisante de l’EGFR, ni la translocation ALK. Cependant, les situations cliniques pour lesquelles les biomarqueurs permettent d'identifier les patients atteints d'un CBNPC métastatique et susceptibles de bénéficier d'une association NIVO + IPI, ne sont pas établies.
L’étude CheckMate 592, dont les principaux résultats ont été rapportés lors de l’édition 2022 de l’ESMO IO, est un essai ouvert de phase II qui explore l'association entre les biomarqueurs et l'efficacité de NIVO + IPI en 1re ligne chez les patients atteints d'un CBNPC métastatique.
Les patients âgés de ≥ 18 ans, atteints d'un CBNPC de stade IV, naïf de traitement ou en récidive et qui avaient un index de performance ECOG de 0 à 1 ont été inclus. Les maladies auto-immunes actives et les métastases cérébrales non traitées étaient exclues.
Dans la 1re partie, 60 patients ont été stratifiés en fonction du statut PD-L1 (≥ 1 % vs < 1 %) avant le traitement.
Dans la 2e partie, 170 patients ont été inclus, quel que soit leur statut PD-L1.
Les patients ont reçu NIVO (240 mg/2 semaines) + IPI (1 mg/kg/6 semaines) jusqu'à 2 ans de traitement ou progression de la maladie, ou toxicité inacceptable.
Le critère d'évaluation principal de la 1repartie est l'association du taux de réponses objectives (TRO) évalué par l’investigateur avec la charge mutationnelle tumorale (CMT) initiale et les biomarqueurs sanguins périphériques et tumoraux candidats à l'inclusion et pendant le traitement ; les critères d'évaluation secondaires sont le TRO, le taux de contrôle de la maladie, la durée de la réponse, le délai de réponse, la survie sans progression (SSP), la survie globale (SG) et l'association des biomarqueurs avec l'efficacité.
Les principaux critères d'évaluation de la 2e partie sont l'association du TRO avec la CMT tissulaire (tCMT) et sanguine (sCMT) à l’inclusion ; les critères d'évaluation secondaires sont le TRO, la SSP, la SG, la tolérance et l'association des biomarqueurs à l'efficacité.
La signature génétique inflammatoire de 4 gènes (CD8A, CD274, STAT-1, LAG-3) a été évaluée dans des échantillons de biopsie à l’inclusion et sous traitement par séquençage d'ARN.
Les caractéristiques des patients à l’inclusion étaient similaires entre la 1repartie et la 2e partie, et dans les sous-groupes tCMT et sCMT.
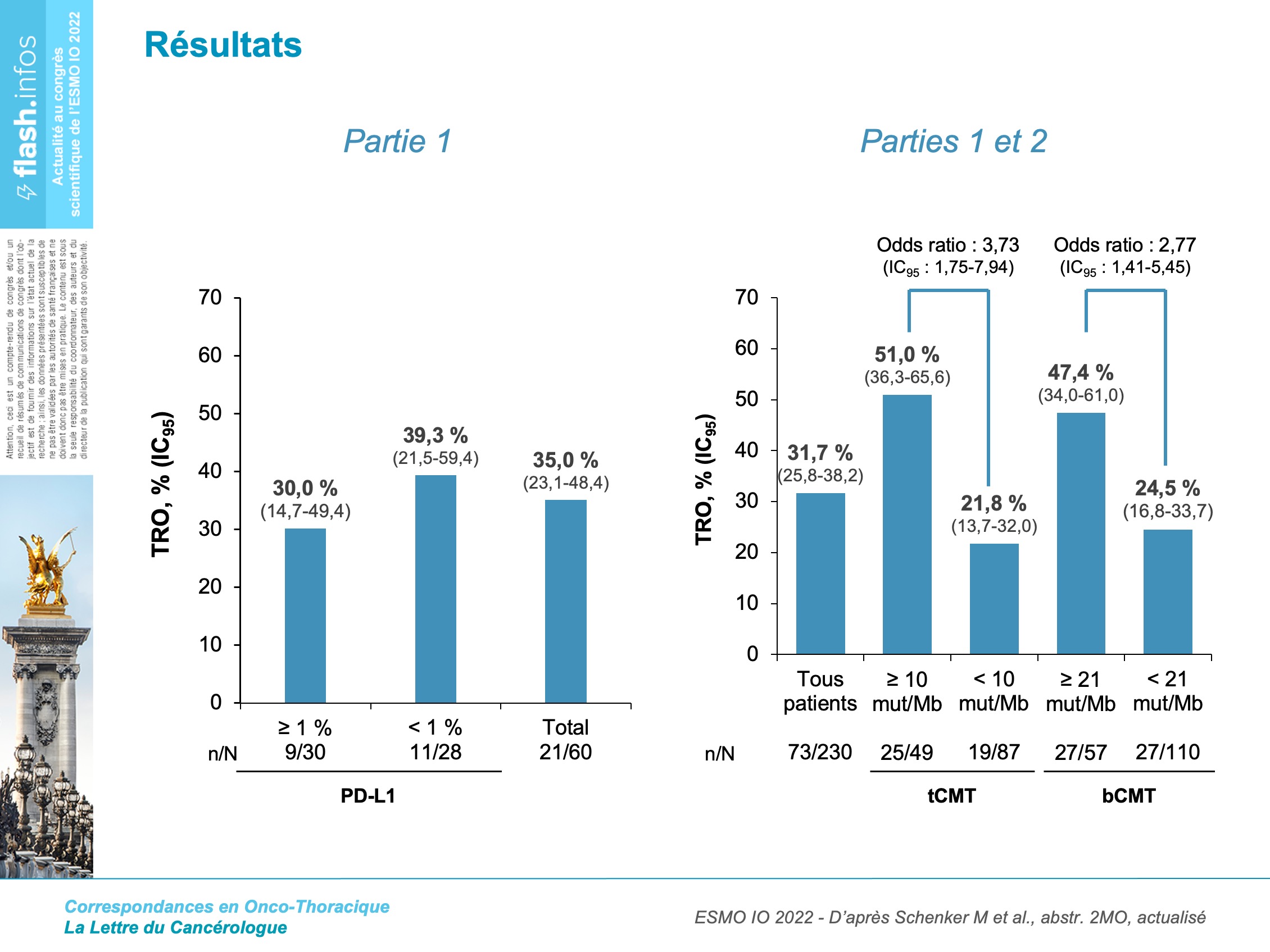
Chez ces patients avec un CBNPC métastatique, traités en 1re ligne par NIVO + IPI, un tCMT élevé (> 10 mut/Mb) ou un sCMT élevé (> 21 mut/Mb) sont associés avec un TRO plus élevé par rapport à une CMT basse. En revanche, le TRO était similaire (figure) dans les cohortes PD-L1 ≥ 1 % ou < 1 % (mais l’interprétation est délicate, car les cohortes étaient de petite taille).
Le score de signature génique inflammatoire à 4 gènes a montré une tendance à l'augmentation sous traitement (n = 17) par rapport à l’inclusion (n = 40) et était numériquement plus élevé chez les répondeurs (réponse complète ou partielle ; n = 13) par rapport aux non-répondeurs (stable ou maladie évolutive ; n = 27 ).
Des événements indésirables de grade 3/4 liés au traitement sont survenus chez 33 % des patients traités. Le profil de tolérance de NIVO + IPI était cohérent avec celui des études précédentes ; aucun nouveau signal de sécurité n'a été observé.
Ces résultats suggèrent une association de la CMT (tissu ou sang) et de la signature inflammatoire à 4 gènes avec l'efficacité clinique de NIVO + IPI en 1re ligne dans le CBNPC métastatique.






