Premier essai randomisé comparant plusieurs immunothérapies ciblant PD-L1, en 1re ligne thérapeutique : résultats de l’essai PERLA avec le dostarlimab
Le pembrolizumab est notre standard thérapeutique en situation de CBNPC, en association à la chimiothérapie en l’absence de sélection sur l’expression de PD-L1 ; le pembrolizumab, comme le cémiplimab – non encore disponible en France dans cette indication –, avait démontré sa supériorité à la chimiothérapie à base de sels de platine seule.
Lors du congrès, les premières données d’un essai randomisé de phase II en double aveugle, comparant un nouvel inhibiteur de PD-1, le dostarlimab, au pembrolizumab, dans le contexte d’associations avec la chimiothérapie pour la 1re ligne thérapeutique des CBNPC, ont été présentées. Dans cette étude PERLA, la population de patients était restreinte aux cancers non épidermoïdes, en 1re ligne, sauf pour les patients avec altération de l’EGFR ou d’ALK, qui pouvaient avoir reçu des thérapies ciblées antérieurement. La chimiothérapie était l’association platine et pémétrexed. Le critère d'évaluation principal était le taux de réponse par un comité de revue indépendant (figure 1).
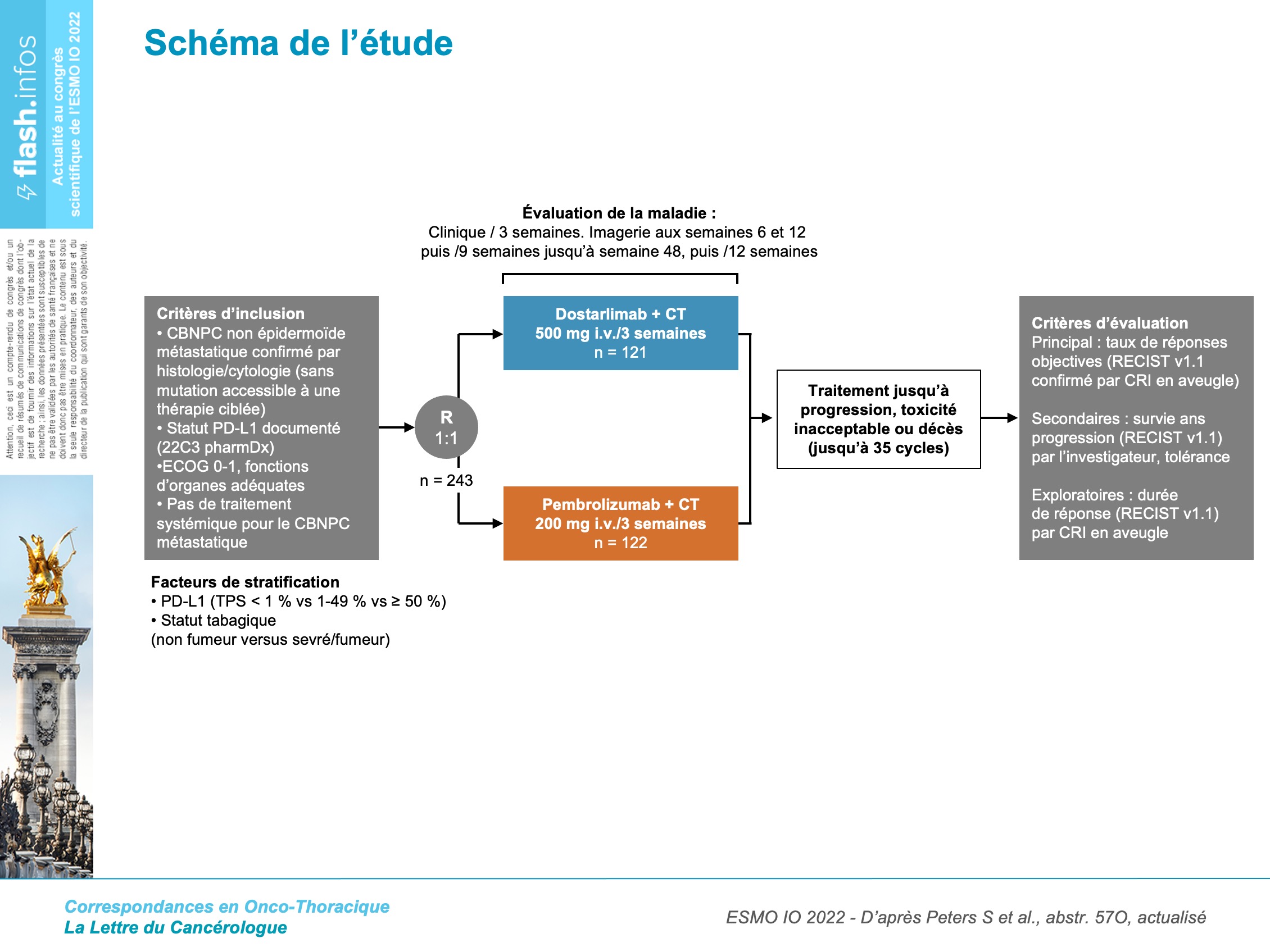
Au total, 243 patients ont été randomisés. La population incluse était semblable à celle des autres essais, avec une répartition équitable de leurs caractéristiques, et environ 40 % de patients avec une expression de PD-L1 négative.
Les résultats montrent un taux de réponse de 46 % dans le bras dostarlimab et de 37 % dans le bras pembrolizumab.
Les médianes de survie sans progression étaient respectivement de 8,8 et 6,7 mois (figure 2).
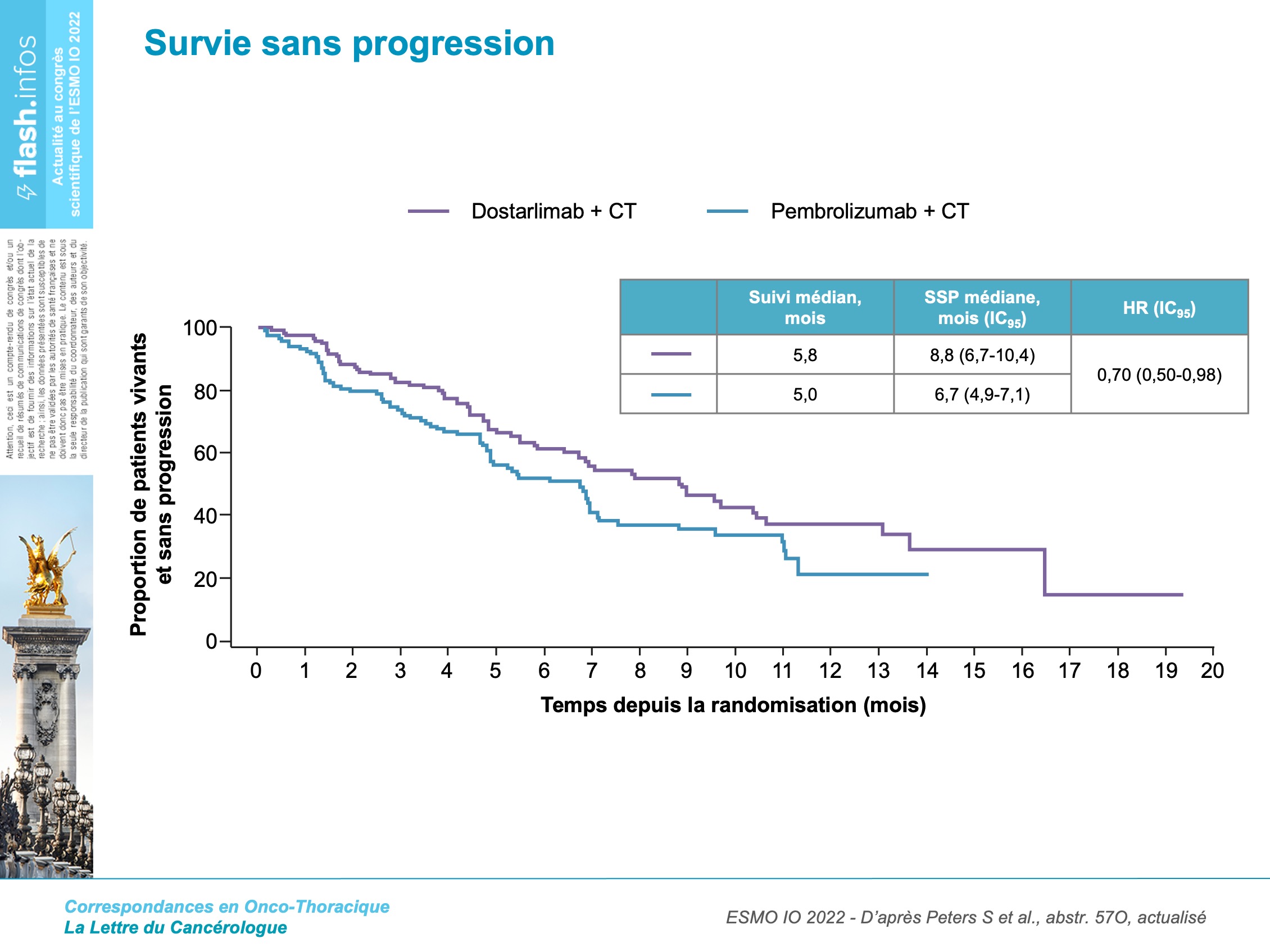
Le critère de jugement secondaire, la réduction de risque de progression, était de 30 % (HR = 0,70 ; IC95 : 0,50-0,98) avec le dostarlimab. Il existait une tendance à une supériorité numérique des taux de réponse et de survie sans progression pour les patients PD-L1 positifs.
Le profil de tolérance était similaire entre les 2 bras.
L’étude a ainsi atteint sont objectif principal d’un taux de réponse sous dostarlimab à plus de 45 %.
Le dostarlimab apparaît ainsi comme une nouvelle option d’immunothérapie associée à la chimiothérapie en 1re ligne, et les résultats présentés montrent que cet agent peut servir de base pour l’évaluation de nouvelles combinaisons thérapeutiques.






