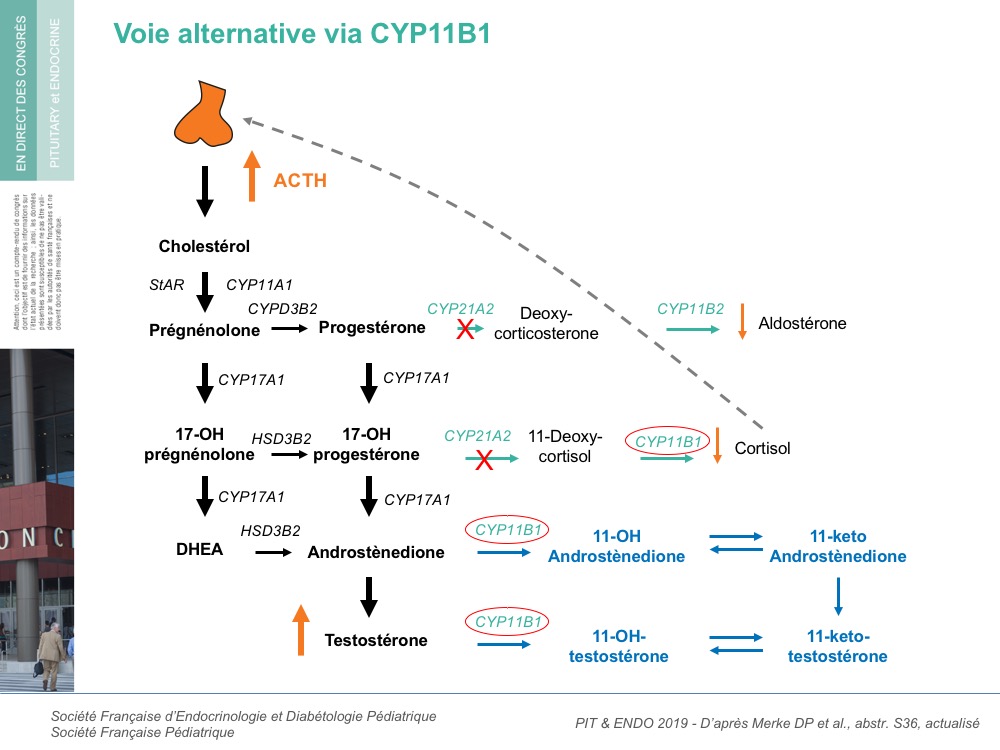
Les androgènes oxygénés sont-ils responsables du phénotype dans l’HCS ?
Le déficit en 21-hydroxylase (CYP21A2) (21OHD) représente plus de 90 % des cas d’hyperplasies congénitales des surrénales (HCS). Les formes classiques de 21OHD sont divisées en 2 groupes : “avec perte de sel” et "virilisante pure”, selon le déficit ou non en minéralocorticoïdes. La gravité de la maladie dépend des mutations sous-jacentes du CYP21A2, l’enzyme métabolisant les stéroïdes nécessaires à la synthèse de l'aldostérone et du cortisol, de son activité résiduelle et de facteurs mal compris, tels que les gènes modificateurs. La diminution de la biosynthèse du cortisol circulant conduit par rétrocontrôle à une forte augmentation de la sécrétion de CRH et d'ACTH, qui provoque une hyperplasie du cortex surrénalien. Le déficit en CYP21A2 entraîne une accumulation des substrats en amont, en particulier de la 17-hydroxyprogestérone (17OHP). Elle est traditionnellement utilisée comme biomarqueur du 21OHD, mais elle présente plusieurs inconvénients : des résultats faussement positifs sont fréquents chez les nouveau-nés prématurés et malades, et des résultats faussement négatifs ont été rapportés lors du dépistage néonatal, en particulier lorsque les mères ont été exposées à des glucocorticoïdes avant la naissance. Afin de surmonter les pièges de l'analyse de la 17OHP, de nouveaux biomarqueurs ont été recherchés :
- le 21-désoxycortisol (21dF), produit hydroxylé en 11β de la 17OHP, est produit uniquement par le cortex surrénalien. Dosé avec la 17OHP après stimulation par le synacthène, le rapport (21dF + 17OHP)/cortisol améliorerait la valeur prédictive positive du dépistage néonatal et du diagnostic de l’hétérozygotie ;
- les organes génitaux atypiques des filles nées avec un 21OHD sont liés à l'excès de 17OHP, dévié par les voies laissées accessibles pour former de puissants androgènes, tels que la testostérone (T). Curieusement, les androgènes mesurés en routine, la DHEA, la DHEA-S, la Δ4A et la T ne sont pas corrélés de façon fiable avec l'excès d'androgènes de ces patientes. C’est peut-être parce que 4 stéroïdes 11-oxygénés, 11OHΔ4, 11KetoΔ4, 11OHT et 11KetoT sont produits. Chez les femmes et les enfants atteints de 21OHD classique, la 11KetoT est l'androgène bioactif dominant dans la circulation.
En résumé, il est probable que des androgènes bioactifs encore mal connus existent et pourront peut-être un jour améliorer le diagnostic et la surveillance des patients porteurs d’HCS.