Inhibiteurs de PI3KCA : fin de partie ?
L'activation de la voie PI3K/AKT est présente dans environ 40 % des cancers du sein RH positif/HER2 négatif, et constitue un facteur de mauvais pronostic en phase métastatique. Après avoir montré un bénéfice en terme de survie sans progression (SSP) dans l’essai SOLAR-1, l’alpélisib était donc devenu le premier inhibiteur de PI3KCA à constituer une option thérapeutique pour nos patientes métastatiques RH+ mutées PI3KCA, après l’échec du tasélisib. L’actualisation récente de cet essai, et notamment les résultats en terme de survie globale (SG), viennent cependant d’entrainer le retrait de l’ATU et d'acter le non-remboursement de cette molécule. Petit retour sur les 2 essais clés des inhibiteurs de PI3KCA.
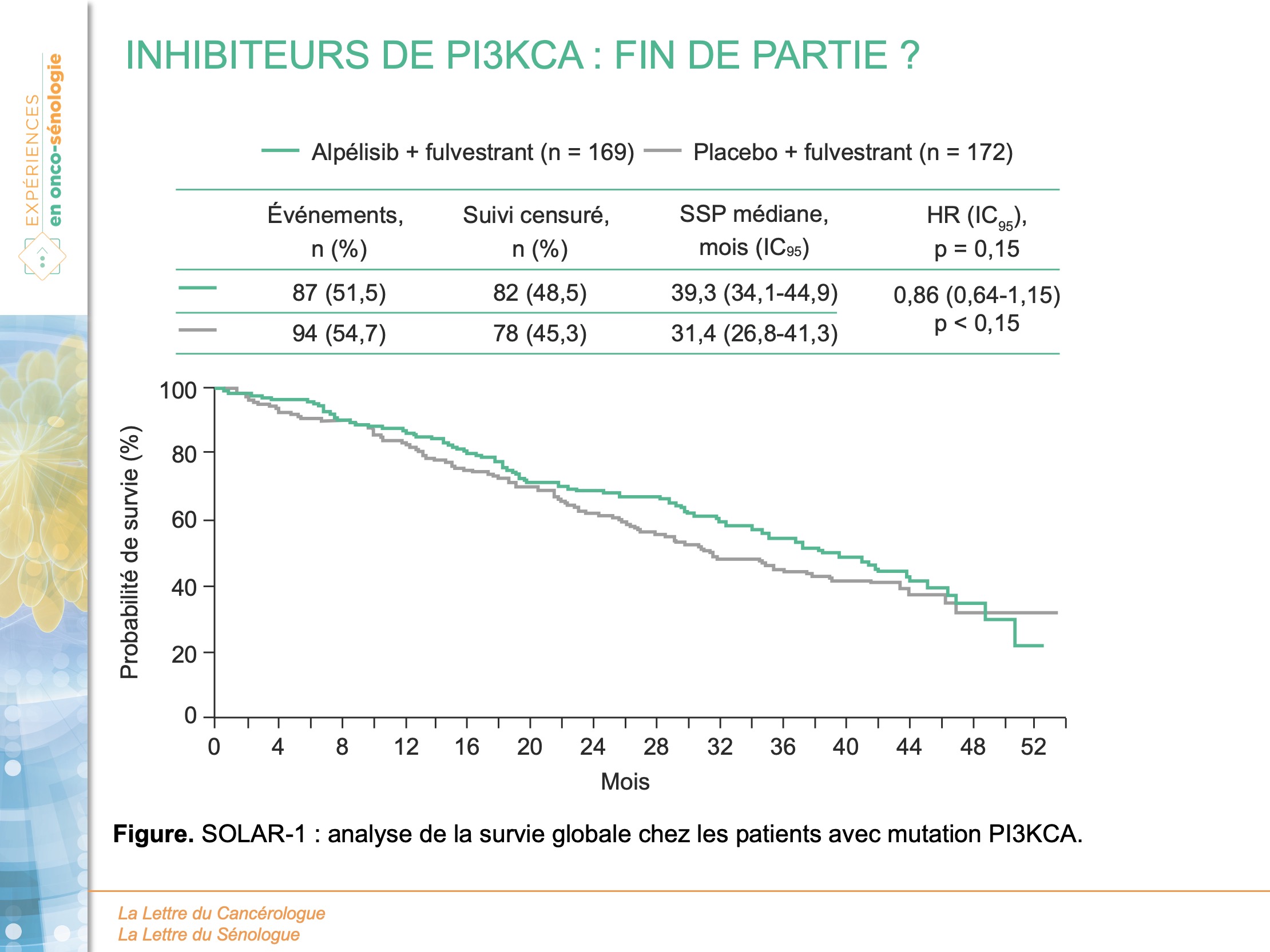
SOLAR-1, essai de phase III, en double aveugle, randomise les patientes ayant rechuté ou progressé sous inhibiteur de l’aromatase entre fulvestrant plus alpélisib (300 mg/jour) versus fulvestrant plus placebo. L’objectif principal est atteint en démontrant une augmentation significative de la SSP dans la population PIK3CA-mutée sur le tissu tumoral : 11 versus 5,7 mois (HR = 0,65 ; IC95 : 0,5-0,85 ; p = 0,00065). Les médianes de SG sont, respectivement dans les 2 bras de 39,3 vs 31,4 mois (figure). Ce différentiel de 8 mois n’est cependant pas statistiquement significatif (HR = 0,86 ; IC95 : 0,64-1,15 ; p = 0,15).
Deux analyses supplémentaires, montrant un bénéfice numérique important de l’alpélisib en SG, ont fait l’objet de discussions bien que les résultats ne soient pas statistiquement significatifs : chez les patients présentant des métastases viscérales (50 % des inclusions), avec un gain en SG de 15 mois (HR = 0,68 ; IC95 : 0,46-1,00) ainsi que chez les patients avec une mutation PIK3CA détectée au niveau de l’ADN tumoral circulant (environ 2/3 des patients de l’étude) avec un gain de 9,2 mois (HR = 0,74 ; IC95 : 0,51-1,08).
La tolérance de l’alpélisib est compliquée, marquée chez 2/3 des patientes par des hyperglycémies (dont 37 % de grade 3-4) et des diarrhées. À noter également, la fréquence des nausées (47 %) et des rashs cutanés (36 %), justifiant une prophylaxie adaptée [1].
Avec un schéma similaire et des critères d’inclusion proches à SOLAR-1, l’essai de phase III SANDPIPER évalue un autre inhibiteur sélectif de PI3KCA, le tasélisib. L’objectif principal est statistiquement atteint mais cliniquement discutable avec une augmentation de la SSP dans la population PIK3CA-mutée de 2 mois avec l’adjonction du tasélisib : 7,4 versus 5,4 mois (HR = 0,70 ; IC95 : 0,56-0,89 ; p = 0,0037). La moitié des patientes traitées par tasélisib présente un effet secondaire de grade 3 (hyperglycémie, diarrhées, rash et nausées), responsable d’un taux plus important d’arrêt de traitement, y compris de l’hormonothérapie [2].
Ce que cet article apporte à ma pratique :
- Augmentation significative de la SSP dans la population PIK3CA-mutée avec l’adjonction de l’alpélisib au fulvestrant après progression sous anti-aromatases (seulement 6 % de la population préalablement exposée aux inhibiteurs de CDK4/6).
- Pas de bénéfice en SG, dans cette même population. Le manque de puissance pour cet objectif secondaire pourrait en être la raison. Le différentiel de 8 mois encourage la réalisation d’études dédiées à la population mutée PI3KCA.
- Profil de tolérance des inhibiteurs de PI3KCA compliqué à manier, nécessitant une prophylaxie par anti-histaminiques et une surveillance rapprochée de la glycémie.
À retenir : Avis défavorable au remboursement de l’alpélisib supprimant l’accès à cette molécule hors essai clinique.
Références
1. André F et al. Alpelisib plus fulvestrant for PIK3CA-mutated, hormone receptor-positive, human epidermal growth factor receptor-2-negative advanced breast cancer: final overall survival results from SOLAR-1. Ann Oncol 2021;32:208-17. doi:10.1016/j.annonc.2020.11.011.
2. Dent S et al. Phase III randomized study of taselisib or placebo with fulvestrant in estrogen receptor-positive, PIK3CA-mutant, HER2-negative, advanced breast cancer: the SANDPIPER trial. Ann Oncol 2021;32:197-207. doi:10.1016/j.annonc.2020.10.596.
















