Vorétigène néparvovec : retour d’expérience
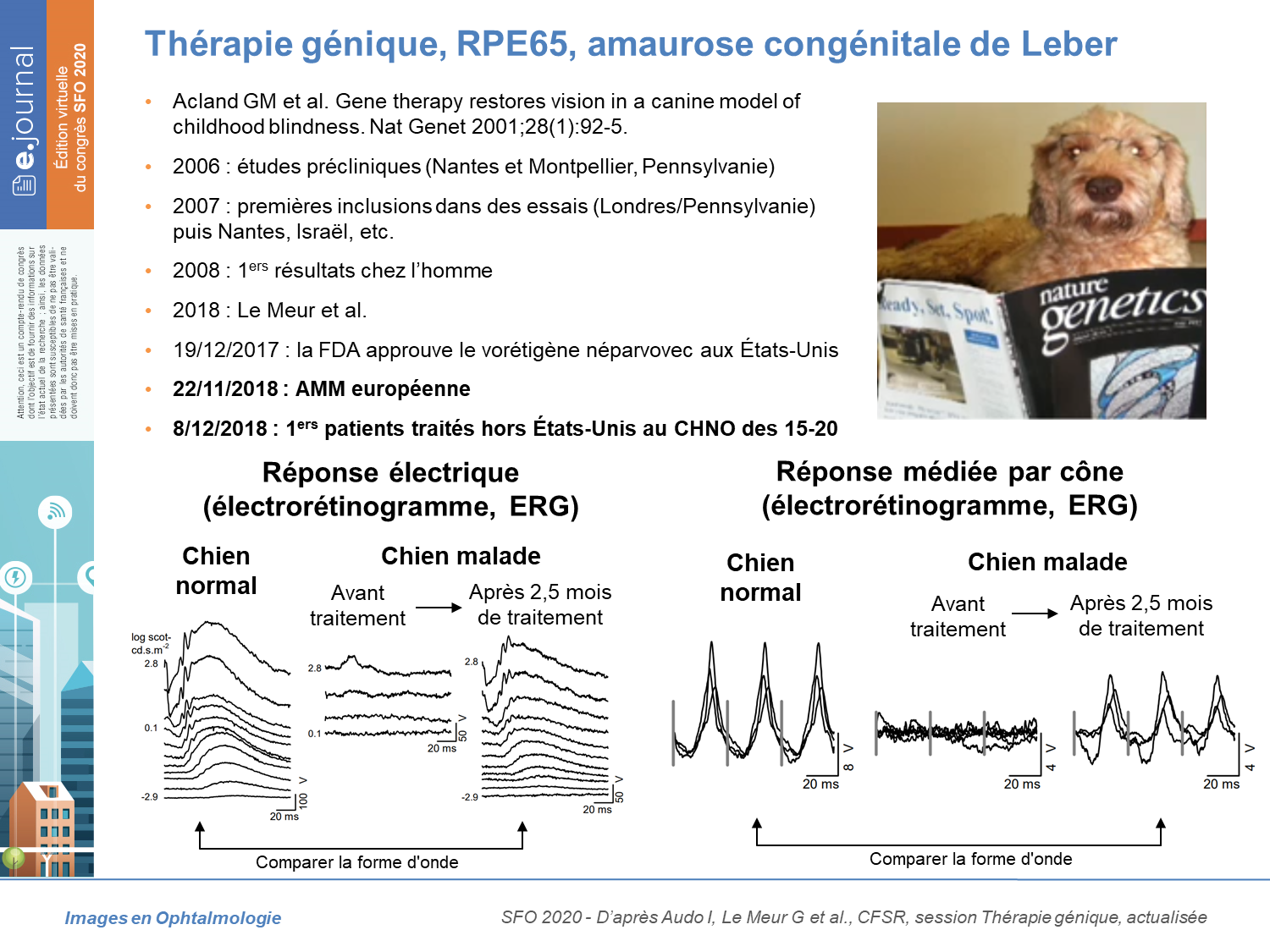
En 2018, le vorétigène néparvovec a été la première thérapie génique commercialisée en ophtalmologie. Elle est destinée aux patients atteints d’amaurose congénitale de Leber ou de rétinopathie pigmentaire liée au gène RPE65. Dans cette pathologie, le cycle visuel de la vitamine A est rompu, la fonction visuelle est faible et l’atrophie rétinienne progresse lentement. Ce décalage entre la perte visuelle précoce et la perte de cellules rétiniennes décalée dans le temps est une fenêtre thérapeutique. Chez des patients présentant suffisamment de cellules rétiniennes viables, ce traitement consiste à injecter 300 µL d’un vecteur viral dans l’espace sous-rétinien après vitrectomie. Cela permet aux cellules de l’épithélium pigmentaire d’exprimer à nouveau le gène RPE65 (figure 1).
Les patients traités présentent une amélioration franche de leur qualité de vie grâce à une amélioration de leurs capacités de déplacement, en particulier dans la pénombre, et à une légère amélioration de l’acuité visuelle. Ce résultat est atteint dès les premières semaines suivant l’injection et est durable sur plusieurs années. Il est également possible, mais pas encore prouvé, que ce traitement permette de ralentir l’évolution de la maladie. À ce jour, on dispose d’un recul de 1 an pour une vingtaine de patients injectés en France (Paris et Nantes) et l’efficacité du traitement a été confirmée par les cliniciens.
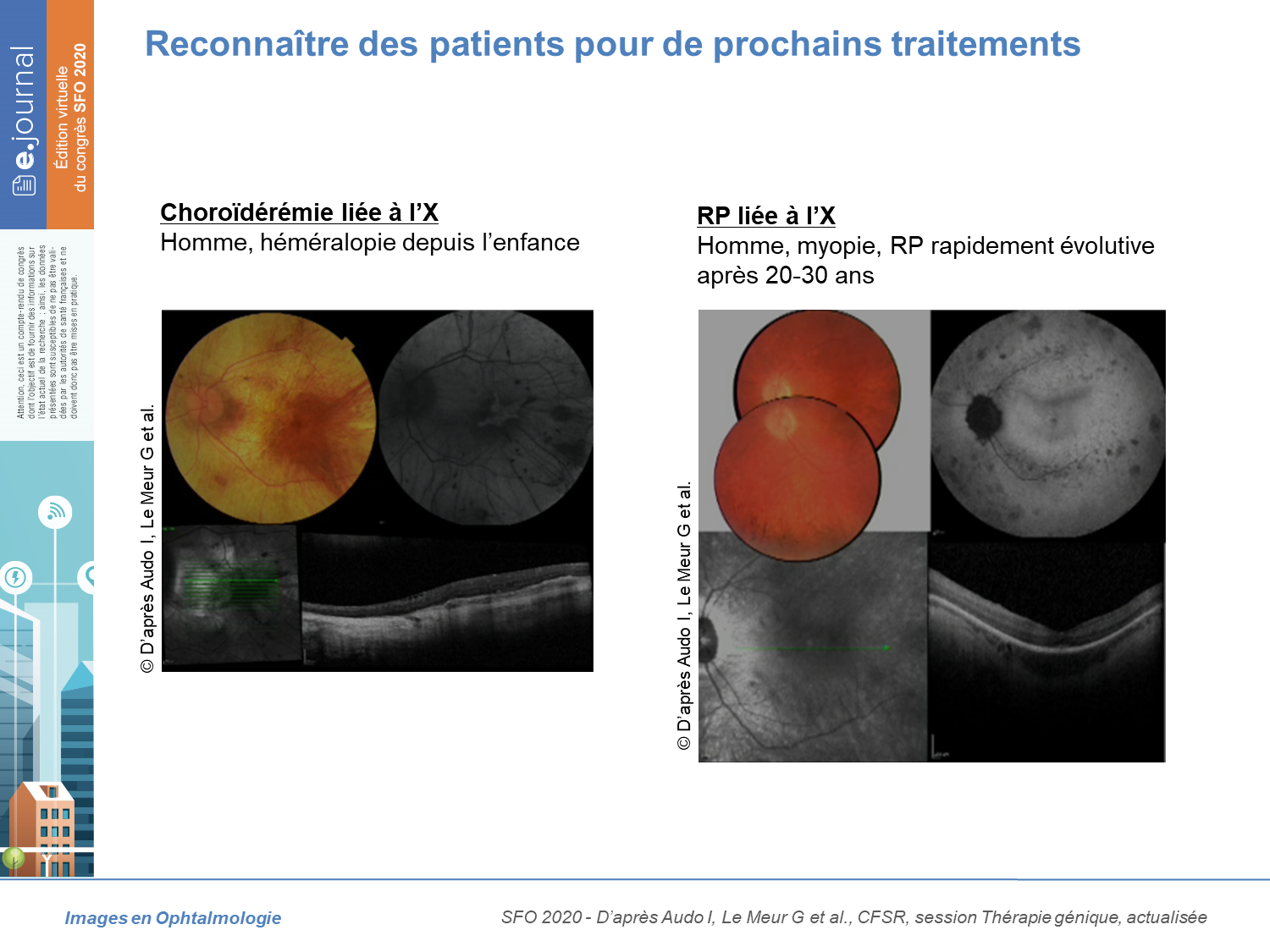
La thérapie génique a fait la preuve de son efficacité. Tout patient atteint d’une dystrophie rétinienne doit avoir une consultation avec génotypage dans un centre de référence pour bénéficier d’un traitement ou se voir proposer une participation à un essai clinique. Les prochaines pathologies qui devraient bénéficier d’un traitement validé sont la choroïdérémie et la rétinite pigmentaire liées à l’X (figure 2).