Inhibiteurs de tyrosine kinase de l’EGFR et insertion de l’exon 20 : osimertinib 160 mg, essai ECOG-ACRIN 5162 de phase II
Les altérations de l’exon 20 de l’EGFR sont les plus fréquentes (≈ 10 %) des mutations rares de l’EGFR. Elles sont très diverses, les plus fréquentes étant :
1. La mutation (rarement isolée) T790M de novo (≈ 1%) traitée par l’osimertinib.
2. La mutation S768I (≈ 1 %) pour laquelle les inhibiteurs de tyrosine kinase (ITK) de 2e et de 3e générations ont une certaine efficacité.
3. Les insertions/duplications de l’exon 20 (4 à 10 %) qui confèrent habituellement une résistance aux ITK et justifient un traitement par doublet de platine. Il existe également une très grande variété de ces ins/del de l’exon 20 que l’on distingue en fonction de leur position dans l’exon 20 (impliquant l’hélice alpha, proche ou loin de la boucle) et de l’implication ou non de la glycine en 770. La résistance aux ITK tient en particulier à une conformation de la poche ATP proche de celle du récepteur sauvage imposant l’utilisation d’ITK également actifs sur le récepteur sauvage et limitant ainsi leur tolérance. Néanmoins, de nombreux ITK ou anticorps spécifiques sont en développement.
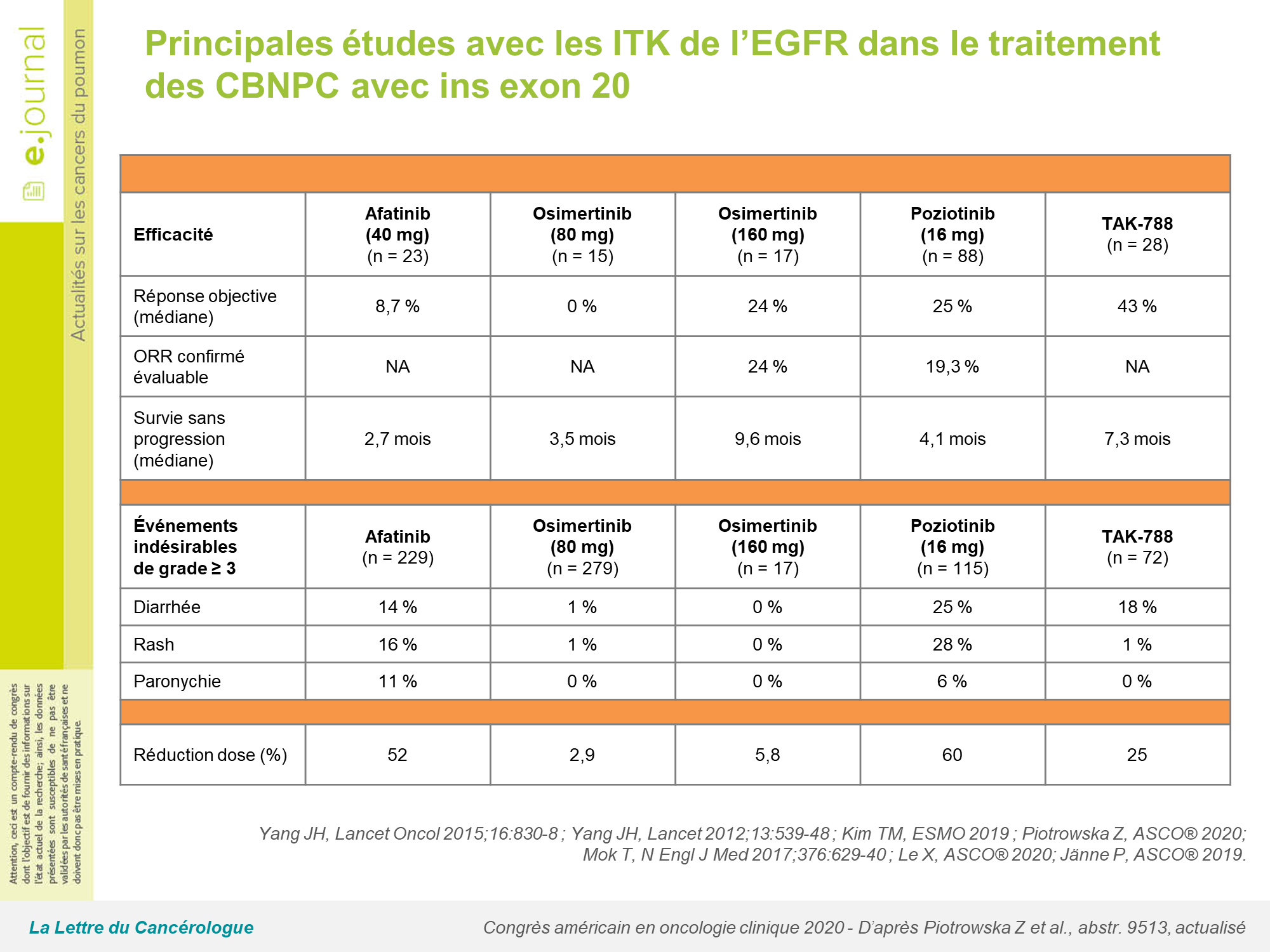
Une première étude (tableau) avec l’osimertinib à la dose de 80 mg s’est avérée décevante. Z. Piotrowaska et al. ont rapporté des résultats intéressants lors de cet ASCO®, dans le cadre de l’essai de phase II EA5162 (NCT03191149) avec l’osimertinib à la dose de 160 mg, chez des patients ayant déjà reçu 1 ligne de traitement. Les patients pouvaient avoir des métastases cérébrales asymptomatiques. Le critère de jugement principal était la réponse objective confirmée en centralisé.
Les résultats ont porté sur 17 patients éligibles, dont 15 évaluables. Il s’agissait plutôt de femmes (71 %), de 65 ans d’âge médian, qui avaient déjà reçu 1 à 3 (2) lignes de traitement. À la date du 14 mai 2020, 24 % avaient présenté une réponse objective et 82 % un contrôle de la maladie. La survie sans progression était de 9,6 mois (4,1-10,7) et la médiane de durée de traitement n’était pas atteinte. La tolérance était excellente, avec un grade ≥ 3 portant sur l’anémie, la mucite ou un allongement du QTc, chez 10, 5 et 10 % des patients, respectivement. Un patient a présenté une pneumopathie interstitielle diffuse de grade 4.
Conclusion
L’osimertinib 160 m/j reste bien toléré et pourrait constituer une option thérapeutique de 2e ligne à évaluer dans le cadre d’un essai thérapeutique. Il pourrait être également évalué en association avec des antiangiogéniques ou des anticorps bispécifiques avec néanmoins un risque de majoration importante de la toxicité. Ces résultats sont à mettre en perspective avec ceux obtenus avec les autres ITK (tableau) et les anticorps bispécifiques (cf. poster discussion 9512, Park K et al., avec l’amivantamab).