Moins de chimiothérapie adjuvante pour les patientes RH+ ? L’actualisation de MINDACT, tout comme TAILORx et RxPONDER, semble nous l’autoriser mais attention pas chez tout le monde !
L’essai MINDACT déjà publié en 2016 avec un suivi médian de 5 ans, vient d’être actualisé dans le Lancet Oncology avec un recul maintenant de 8,7 ans (1).
Cet essai de phase III pose la question de l’utilisation d’une signature génomique – en l’occurrence le test MammaPrint® de 70 gènes – pour sélectionner une population de patientes avec un cancer du sein RH+ éligible à une désescalade de leur stratégie adjuvante, c’est-à-dire avec le maintien d’un seul traitement systémique : l’hormonothérapie (2). Le schéma de cette étude est rappelé dans la figure 1.
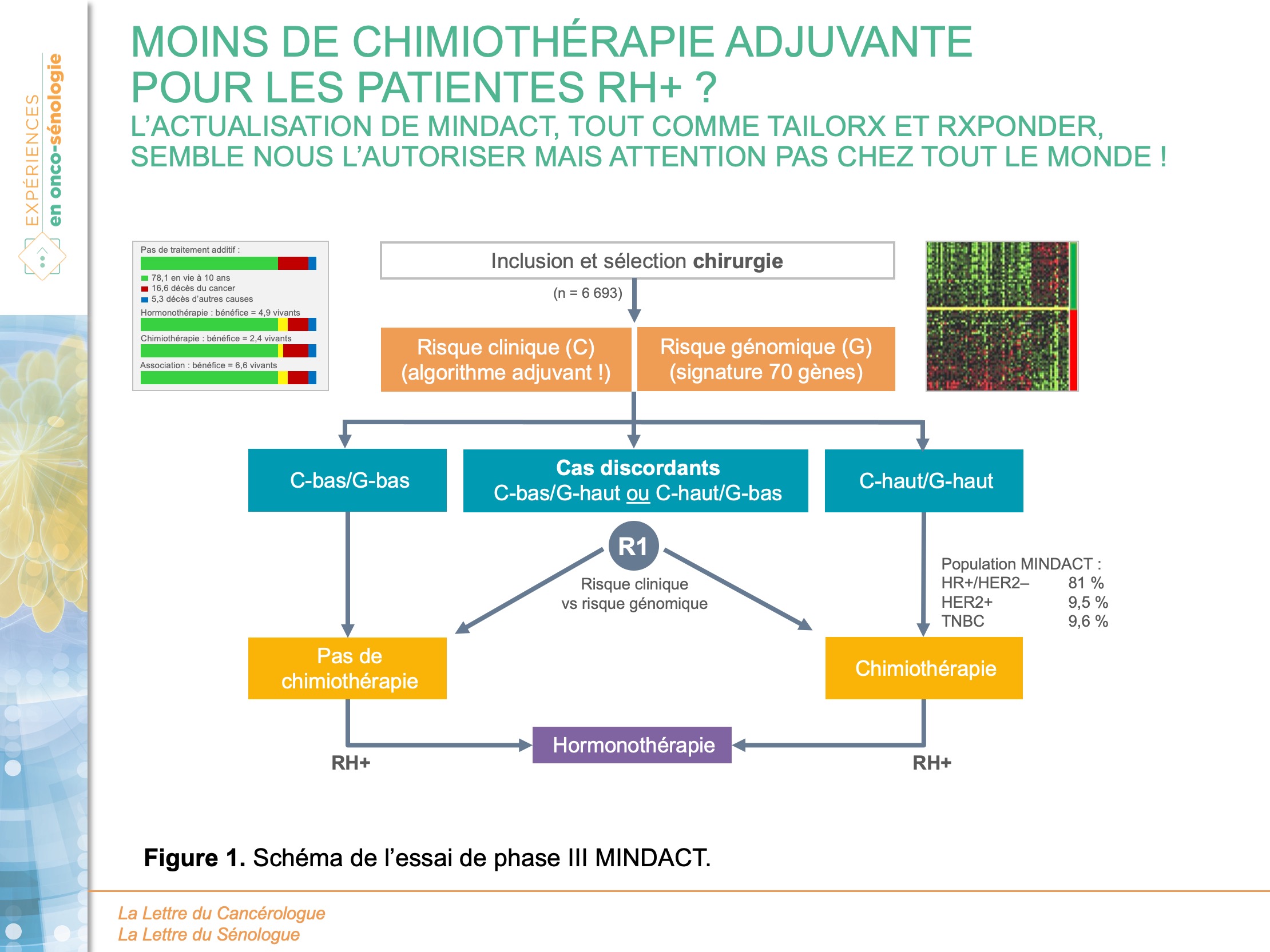
Près de 6 700 patientes ont participé à ce large essai prospectif. La population d’intérêt particulier correspond aux patientes présentant des résultats dissociés : un score clinique élevé [C-high] (évalué par Adjuvant Online) mais un score génomique bas [G-low]. Avec une médiane de suivi de plus de 8 ans, les résultats de survie sans récidive à distance (SSRD) à 5 ans, objectif principal de l’étude, restent identiques à ceux publiés préalablement : 95,1 % (2)(figure 2). Cette donnée pourrait donc autoriser chez des patientes C-high, ayant donc une indication théorique de chimiothérapie adjuvante, à proposer une hormonothérapie seule en cas de score moléculaire bas.
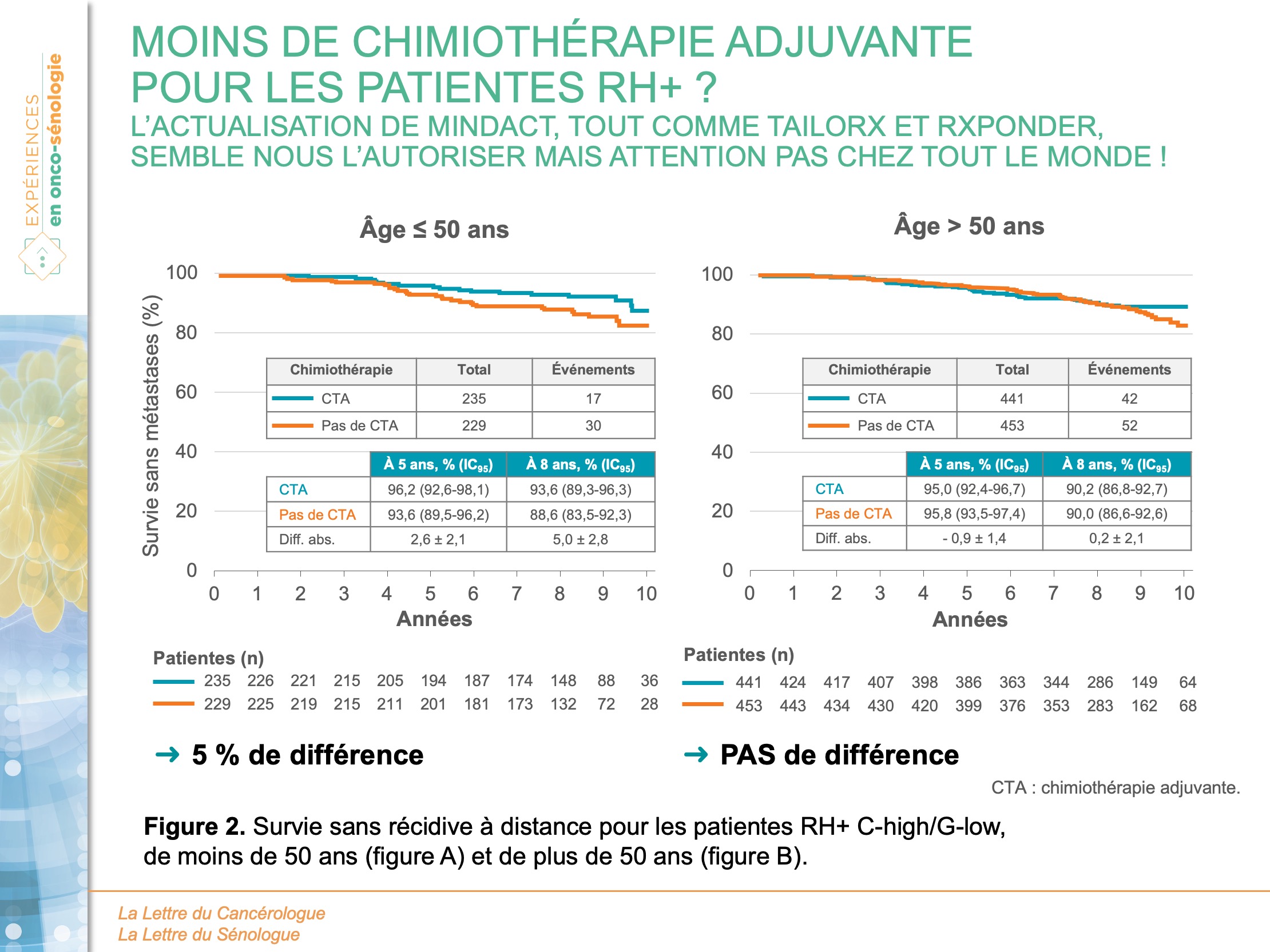
Deux éléments viennent cependant nuancer cette conclusion :
- Dans cette même population, la SSRD à 8 ans est de 92 % pour le bras chimiothérapie-hormonothérapie et 89,4 % pour le bras hormonothérapie seule (HR = 0,66 ; IC95 : 0,48-0,92). Ce différentiel de 2,6 % (non décrit à 5 ans) reste cependant à mettre en perspective avec la toxicité certaine d’une chimiothérapie adjuvante, et ne semble donc pas suffisant pour remettre en question cette possibilité de désescalade.
- Les résultats en fonction de l’âge des patientes (avant ou après 50 ans) viennent confirmer les données de TAILORx et RxPONDER (OncotypeDx) sur l’intérêt de la chimiothérapie chez les femmes non ménopausées (3, 4). Pour les femmes de moins de 50 ans, apparait clairement un avantage à l’ajout de la chimiothérapie adjuvante avec un SSRD à 8 ans de 88,6 % (IC95 : 83,5-92,3) sans chimiothérapie contre 93,6 % (IC95 : 89,3-96,3) avec chimiothérapie. Il est important de noter que seules 16,2 % des patientes sous HT seule et 26,4 % des patientes ayant reçu de la chimiothérapie ont bénéficié d’un traitement par analogue de la LHRH en association avec le tamoxifène.
Ce que cet article apporte à ma pratique
- L’essai MINDACT confirme l’intérêt de la signature génomique MammaPrint® pour s’abstenir d’une chimiothérapie adjuvante.
- Cette proposition d’abstention est à envisager, si la signature est favorable (G-low), pour les patientes avec un cancer du sein RH+, y compris avec envahissement ganglionnaire (jusqu’à 3N+) de plus de 50 ans.
- Il existe un bénéfice de la chimiothérapie adjuvante chez les moins de 50 ans, directement lié au bénéfice intrinsèque des molécules utilisées ou indirectement via l’effet de suppression ovarienne chimio-induite.
À retenir
- La signature génomique Mammaprint® représente un outil robuste d’aide à la désescalade des indications de chimiothérapie adjuvante chez les patientes RH+ ménopausées.
- Quid cependant des autres tests génomiques, utilisé en routine clinique ? Peut-on réellement extrapoler les données de TAILORX, RxPONDER et MINDACT à toutes les signatures ?
Références
1. Piccart M et al. 70-gene signature as an aid for treatment decisions in early breast cancer: updated results of the phase 3 randomised MINDACT trial with an exploratory analysis by age. Lancet Oncol 2021;22:476-88.
2. Cardoso F et al. 70-gene signature as an aid to treatment decisions in early-stage breast cancer. N Engl J Med 2016;375:717-29.
3. Sparano JA et al. Adjuvant chemotherapy guided by a 21-gene expression assay in breast cancer. N Engl J Med 2018;379:111-21.
4. Kalinsky K et al. First results from a phase III randomized clinical trial of standard adjuvant endocrine therapy (ET)+/-chemotherapy (CT) in patients (pts) with 1-3 positive nodes, hormone receptor-positive (HR+) and HER2-negative (HER2-) breast cancer (BC) with recurrence score (RS)< 25: SWOG S1007 (RxPonder). San Antonio Breast Cancer Symposium 2020.
















