Activité des ITK dans les CPNPC avec métastases leptoméningées
Bien que sous-diagnostiquées, les métastases leptoméningées (ML) surviennent chez 10 % des patients atteints d’un carcinome pulmonaire non à petites cellules (CPNPC) avec mutation du gène de l’EGFR, ce qui entraîne des résultats décevants, avec une survie qui ne dépasse pas 1 an.
Dans cet article, R. Flippot et al. (1) explorent l’activité des inhibiteurs de tyrosine kinase (ITK) qui ciblent le récepteur de l’EGF dans une cohorte de patients atteints d’un CPNPC avec des ML après échec d’un ITK. Il s’agit d’une étude rétrospective internationale multicentrique portant sur 92 patients atteints d’un CPNPC EGFR positif et ML, diagnostiqués entre août 2003 et octobre 2018. L’échec de l’ITK a été caractérisé comme : diagnostic de ML au cours d’un traitement systémique par ITK ou progression de ML connue au cours du traitement par ITK. La reprise de l’ITK a été définie comme une nouvelle ligne de thérapie ciblée après échec, y compris l’administration d’autres ITK ou l’adaptation du schéma posologique (par exemple l’augmentation de la posologie).
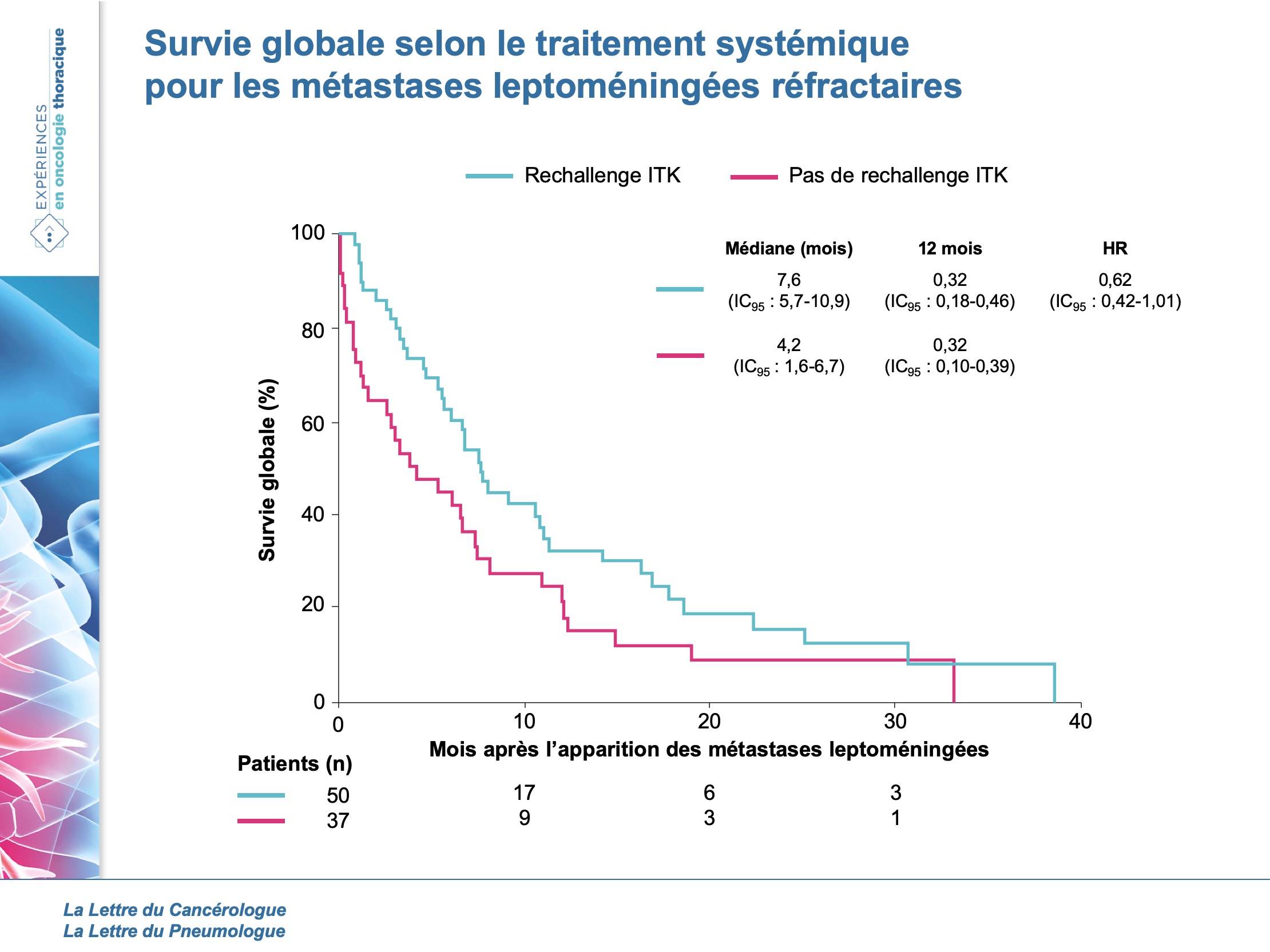
Dans l’ensemble de la population, la survie globale (SG) depuis le diagnostic de ML était de 6,1 mois (IC95 : 4,2-7,6) et le taux de SG à 12 mois était de 27 % (IC95 : 18-37). La progression sous ITK s’est produite chez 87 patients et 50 (57 %) ont bénéficié d’une nouvelle ligne par un ITK. La SG depuis le diagnostic de ML chez les patients traités par une nouvelle ligne d’ITK était de 7,6 mois (IC95 : 5,7-10,9), comparativement à 4,2 mois (IC95 : 1,6-6,7) chez les patients sans autre traitement (figure). La plupart des patients (60 %) avaient changé d’ITK, tandis que 40 % ont été traités avec la même thérapie, mais à dose plus intense, visant à augmenter la diffusion méningée (34 %).
La réponse clinique et les bénéfices cliniques ont été observés chez 28 et 60 % des patients, respectivement. L’erlotinib était la thérapie ciblée le plus fréquemment utilisée pour la reprise d’un ITK chez 22 des 50 patients (44 %). Dix-sept patients (34 %) ont reçu des schémas posologiques intensifiés lors de la reprise de l’ITK. Parmi ceux-ci, 6 sur 17 (35 %) ont eu une réponse clinique et 10 sur 17 (59 %) un bénéfice clinique.
En conclusion, la reprise ou la modification d’un traitement par ITK après un échec se montre potentiellement efficace sur les ML. Des taux de réponse élevés ont été observés chez les patients qui ont reçu de l’erlotinib après un ITK de 1re ou de 2e génération. Cette étude montre qu’une stratégie utilisant diverses lignes d’ITK entraîne un avantage significatif de la SG chez les patients atteints des ML. Le changement du médicament ou les stratégies utilisant des doses plus élevées peuvent aider à contourner la résistance aux ITK dans un contexte d’une progression méningée et à améliorer la survie.
Ce que cet article apporte à ma pratique :
- Environ 10 % des patients avec un CPNPC présentant une mutation du gène EGFR développent des ML.
- Les auteurs ont évalué l’activité des ITK chez une cohorte de 92 patients atteints d’un CPNPC EGFR muté avec ML après un échec par ITK.
- La SG après diagnostic de ML était de 6,1 mois et le taux de SG sur 12 mois était de 27 %.
- 57 % des patients ont bénéficié d’un rechallenge avec un ITK ; dans la plupart des cas il s’agit d’un changement de traitement mais dans 40 % des cas avec le même traitement mais à des doses plus élevées.
- Des taux de réponse élevés et un bénéfice prolongé ont été observés chez les patients qui ont reçu de l’erlotinib après une ITK de 1re ou de 2e génération, ou qui ont reçu une dose élevée d’erlotinib.
- Les données actuelles soutiennent l’utilisation de l’ITK à dose élevée de secours au moment de l’échec du traitement à dose normale chez les patients atteints de ML et EGFR mutés. Toutefois, cette stratégie ne devrait être envisagée que chez les patients atteints d’une maladie en progression méningée.
- ITK à forte dose : une option dans les atteintes leptoméningées des CPNPC EGFR+.
Références
1. Flippot R et al. Activity of EGFR tyrosine kinase inhibitors in NSCLC with refractory leptomeningeal metastases. J Thoracic Oncol 2019;14(8):1400-7.
















