Étude CodebreaK 100 : bénéfice clinique chez les CBNPC avancés traités par le sotorasib (AMG 510)
Le sotorasib est un inhibiteur du KRASG12C. Un essai de phase I a montré un profil de sécurité favorable et une activité antitumorale préliminaire chez les patients atteints de tumeurs solides avancées porteuses de KRAS p.G12C. L’étude CodebreaK 100 a quant à elle évalué la durabilité du bénéfice clinique et les biomarqueurs dans différentes tumeurs dont les CBNPC. Les principaux critères d'éligibilité comprenaient la mutation KRAS p.G12C et la nécessité d’un traitement systémique préalable. Le critère d'évaluation principal était la sécurité ; les principaux critères d’évaluation secondaires étaient le taux de réponse objective, le taux de contrôle de la maladie, la durée de la réponse et la survie sans progression (SSP). La fréquence de l’allèle mutant KRAS p.G12C et le niveau de PD-L1 ont été également examinés.
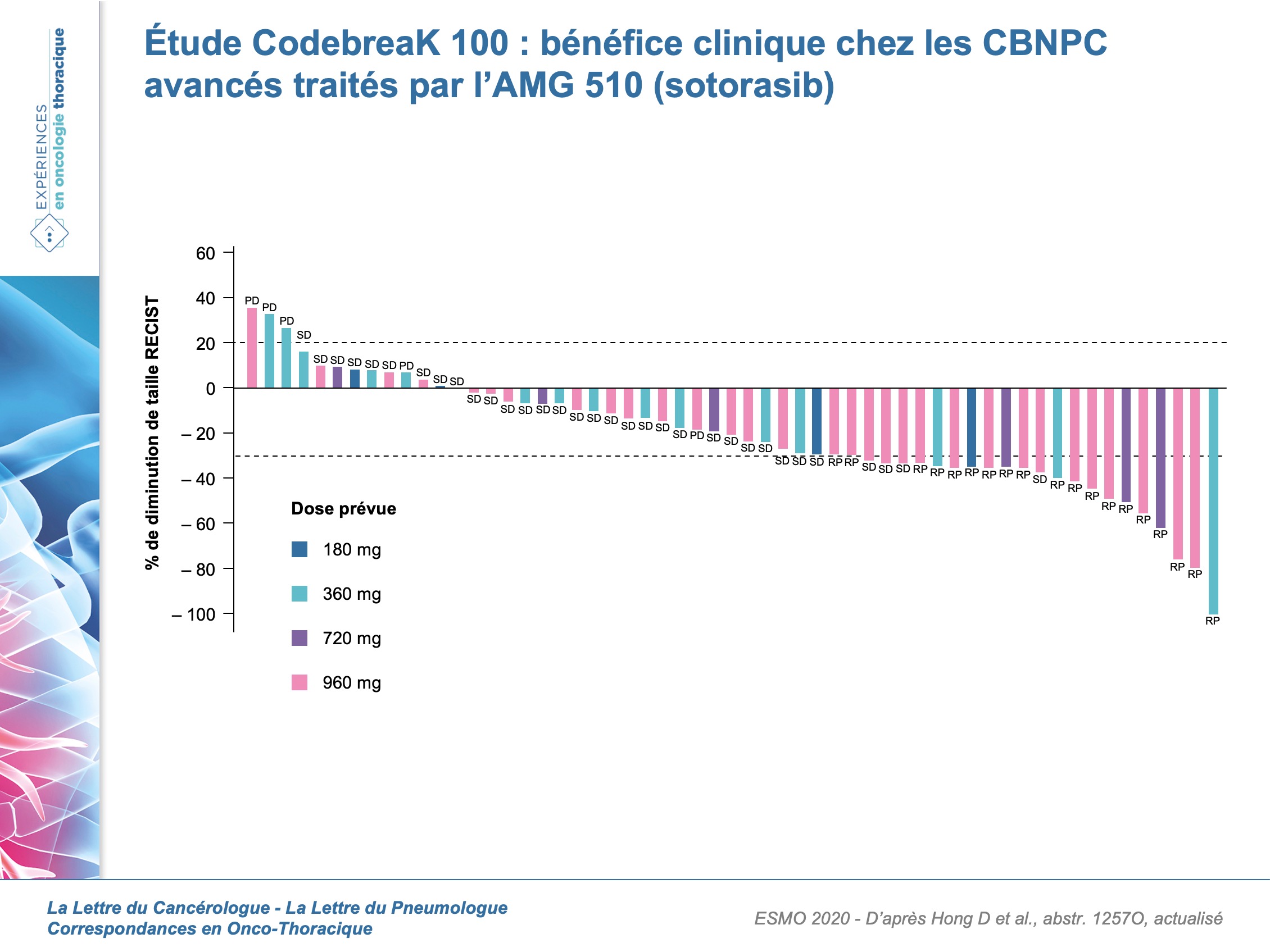
Au moment de l’évaluation au 1er juin 2020, 59 CBNPC (35 femmes [59,3 %] ; âge médian : 68,0 ans [49-83]) étaient inclus dans l’étude. 44 (74,5 %) et 30 patients (50,8 %) ont reçu ≥ 2 et 3 lignes de traitement préalables, respectivement. Le suivi médian était de 11,7 mois (IC : 4,8-21,2). Cinq patients (8,5 %) ont eu des effets indésirables conduisant à l'arrêt du traitement. Il n’y a pas eu de toxicité limitante, ni d'événements indésirables mortels liés au traitement. La SSP médiane était de 6,3 (IC95 : 0-14,9) mois. Le taux de réponse objective était de 35,3 % (IC95 : 19,8-53,5) (figure). La durée de la réponse médiane était de 10,9 mois (1,1-13,6). Le taux de contrôle de la maladie était de 88,1 % (IC95 : 77,1-95,1). Chez 32 patients, les données sur la fréquence des allèles mutants étaient disponibles pour KRAS p.G12C (9 réponses partielles, 19 maladies stables, 2 progressions). Il n’y avait pas d’association significative entre la fréquence de l’allèle mutant et la réponse (Wilcoxon p = 0,43 pour RP vs SD). Dix-huit patients étaient évalués pour le PD-L1. Le score médian de PD-L1 [TPS] était non associé à la réponse (Wilcoxon p = 0,73 pour RP vs SD), pas plus que le TMB ou les comutations.
Ce que cet article apporte à ma pratique :
- Chez les sujets atteints d’un CBNPC lourdement prétraité, des réponses durables au sotorasib ont été observées, la majorité des sujets ayant eu un contrôle de la maladie.
- Les données actuelles sur un nombre limité de patients suggèrent que ni la fréquence des allèles mutants de KRAS p.G12C ni l’expression de PD-L1, le TMB ou les comutations ne permettent de prédire la réponse au sotorasib.
















