Inhibiteurs de checkpoint dans les CBNPC : facteurs prédictifs de réponse
L’expression de PD-L1 et le tumor mutational burden (TMB) ne semblent pas parfaits pour prédire une réponse aux ICI. De plus, le séquençage exomique prend en compte des mutations n’engendrant que peu de néoantigènes. Récemment, des marqueurs moléculaires comme STK11, PTEN, KRAS, TP53 et les différents drivers oncogéniques connus ont montré des réponses différentes en fonction de leur présence ou non. L’expression the tissue is the issue revêt tout son sens dans les CBNPC, cependant la difficulté d’accès, sa qualité et sa faible représentativité de l’hétérogénéité de la tumeur rendent les analyses difficiles.
Cette étude (1) a pour but de vérifier l’utilité de la détection de l’ADN tumoral circulant (ctDNA) sanguin, qui semble plus représentatif de la tumeur, en se focalisant sur ces dernières mutations pour créer un score pronostique afin d’identifier les répondeurs mais également d’évaluer si les changements d’expression de ce ctDNA en cours de traitement peut prédire le maintien de la réponse.
Les auteurs ont étudié 36 gènes par NGS avant inhibiteurs de checkpoint immunitaire (ICI) puis à 1 mois du traitement. Pour le changement d’expression du ctDNA en cours de traitement, les auteurs ont sélectionné une seule mutation somatique.
Parmi les 187 patients de la cohorte IMMUNOPREDICT, 86 étaient utilisables. 39 étaient des répondeurs (SSP > 6 mois et réponse à la première évaluation) et 47 étaient non-répondeurs (progression à la première évaluation).
Il y avait 62 % d’hommes, 74,2 % de patients atteints d’adénocarcinome, 22,7 % de fumeurs actifs, 88,7 % de stade 4 et 100 % ont eu de la chimiothérapie auparavant. L’ICI prépondérant était le nivolumab dans 92,8 % des cas.
La SSP médiane totale était de 7 mois. Cependant, ceux qui n’avaient aucune mutation avaient une SSP de 3,5 mois, ceux qui présentaient un driver oncogénique (ALK = 1 et EGFR = 5) avaient une SSP médiane de 2 mois (après avoir reçu des TKI en lignes précédentes). Mais surtout les mutés PTEN ou STK11 présentaient une survie diminuée comparés aux non-mutés alors que ceux ayant une transversion dans KRAS ou TP53 étaient plus sensibles (figures 1 et 2).
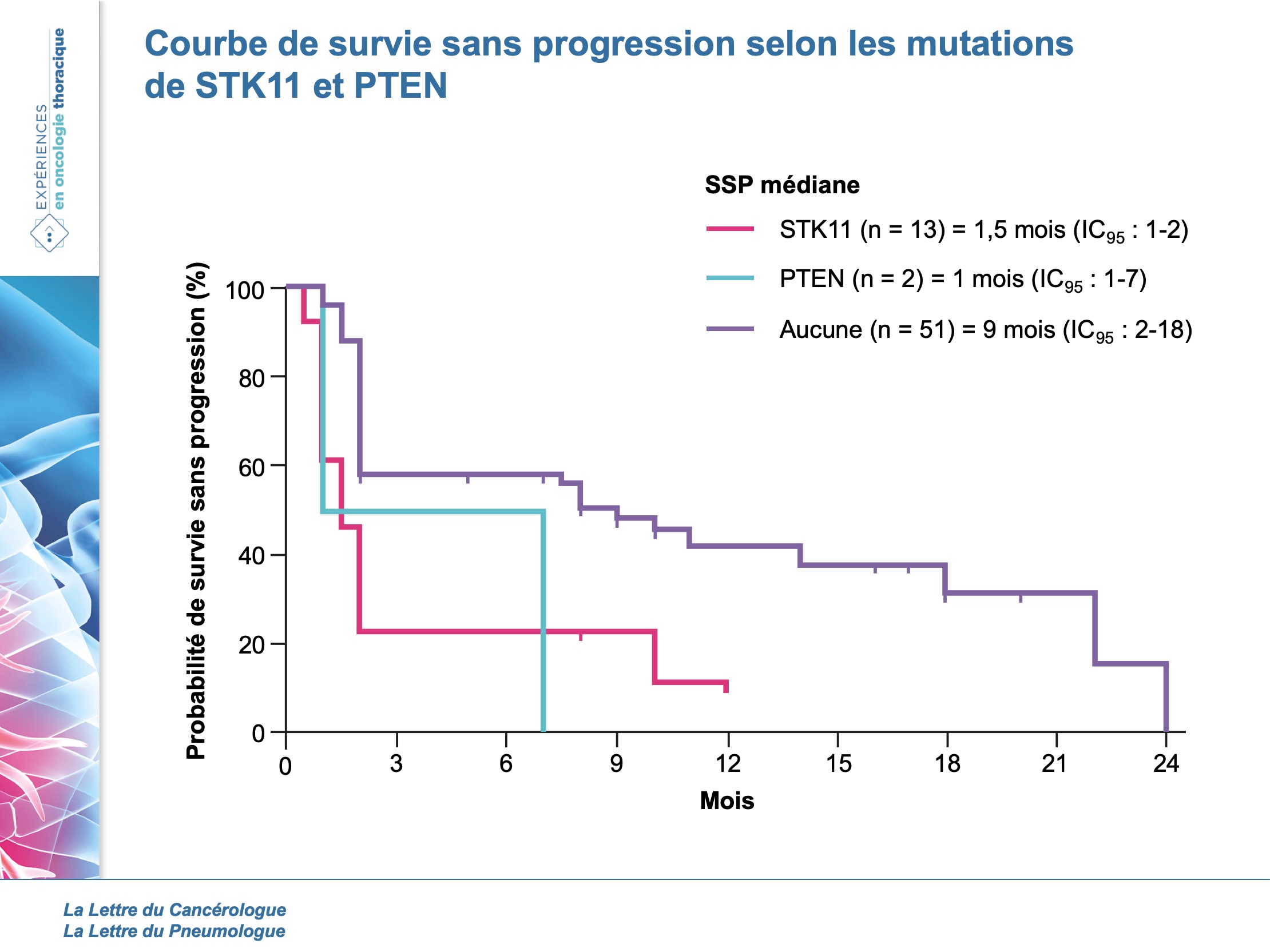
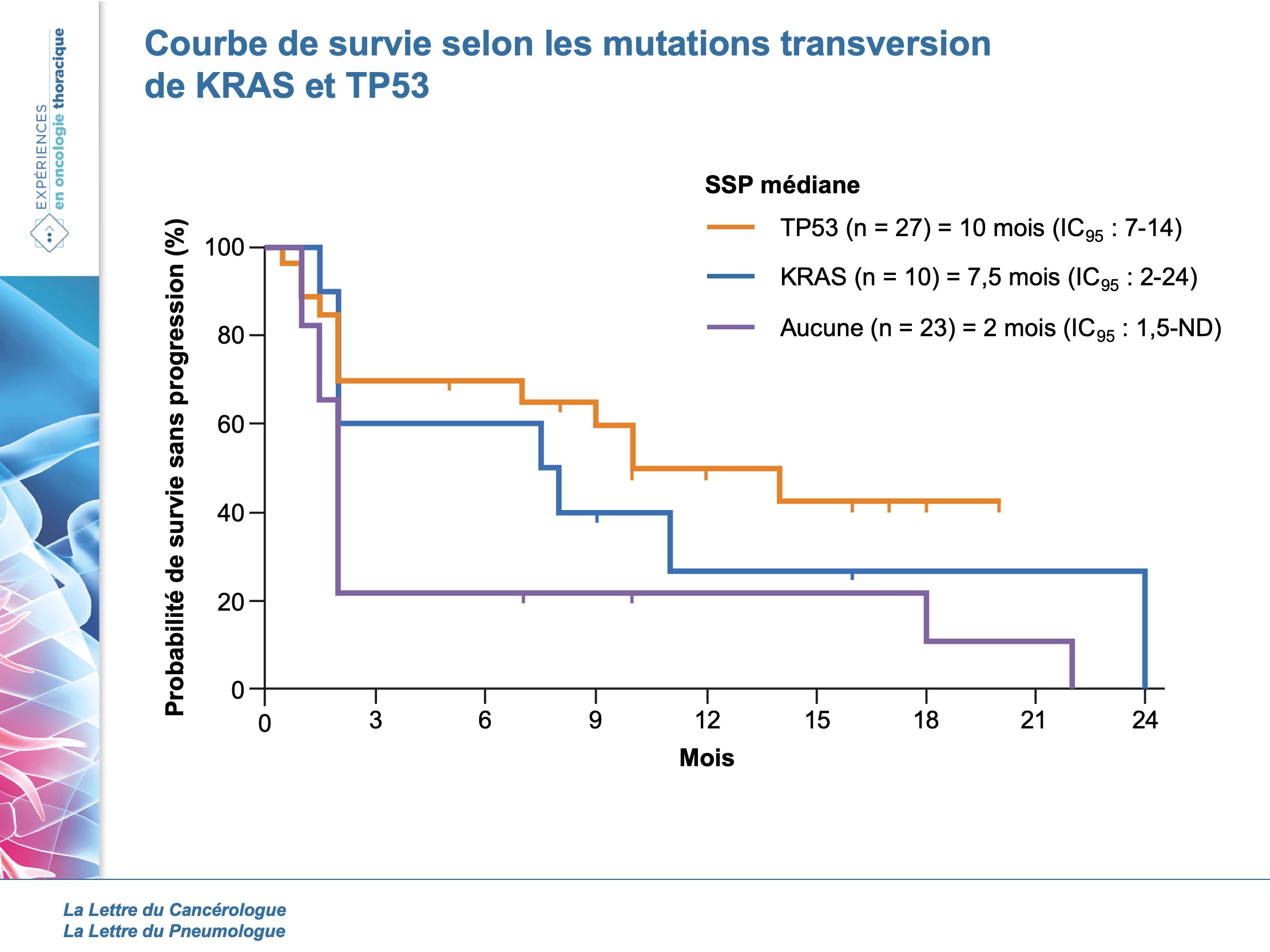
Les auteurs ont ainsi pu élaborer un algorithme en fonction de ces anomalies pour choisir le traitement le plus adapté, en les séparant en 3 groupes distincts aux survies différentes (figures 3 et 4).
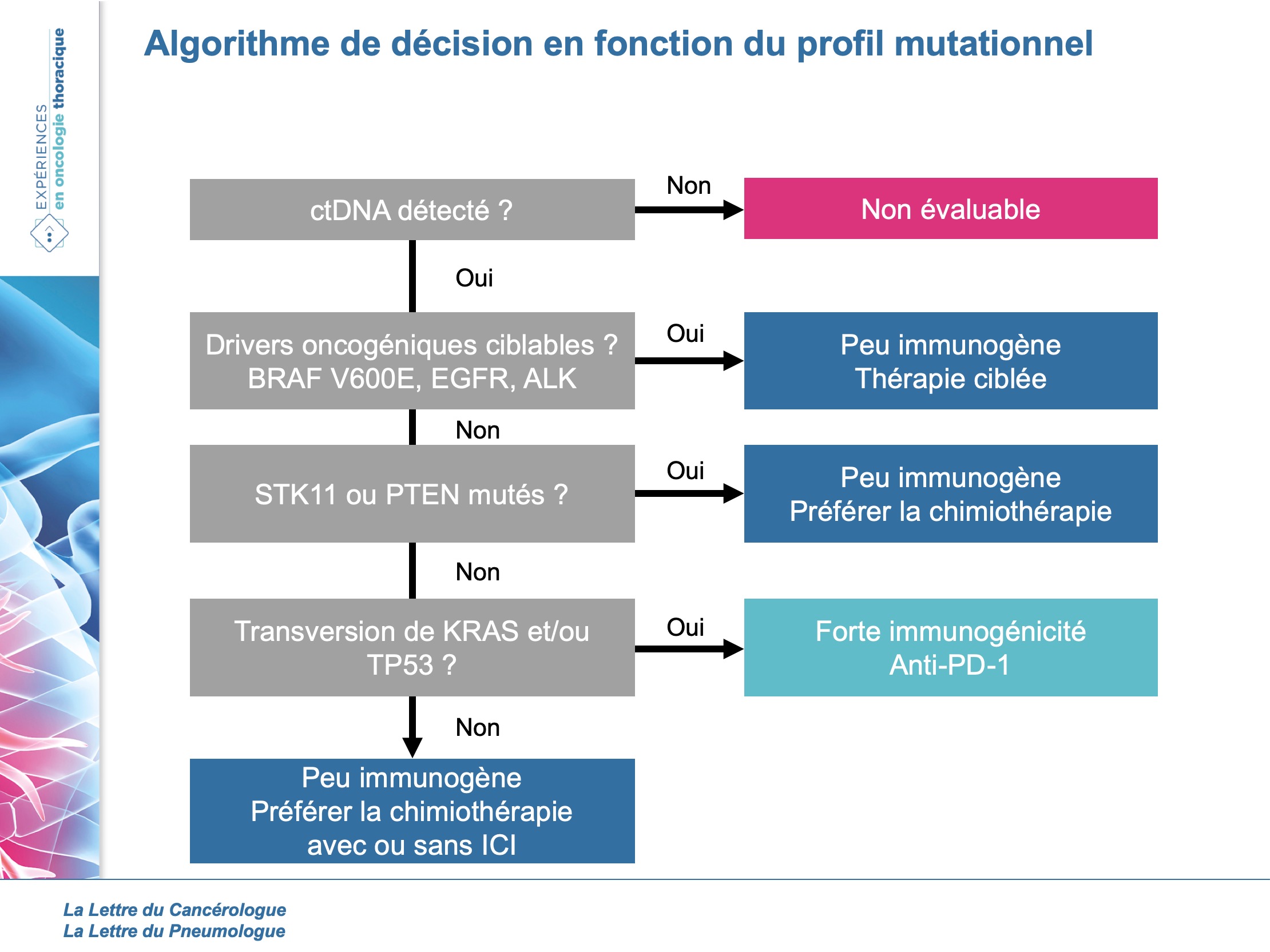
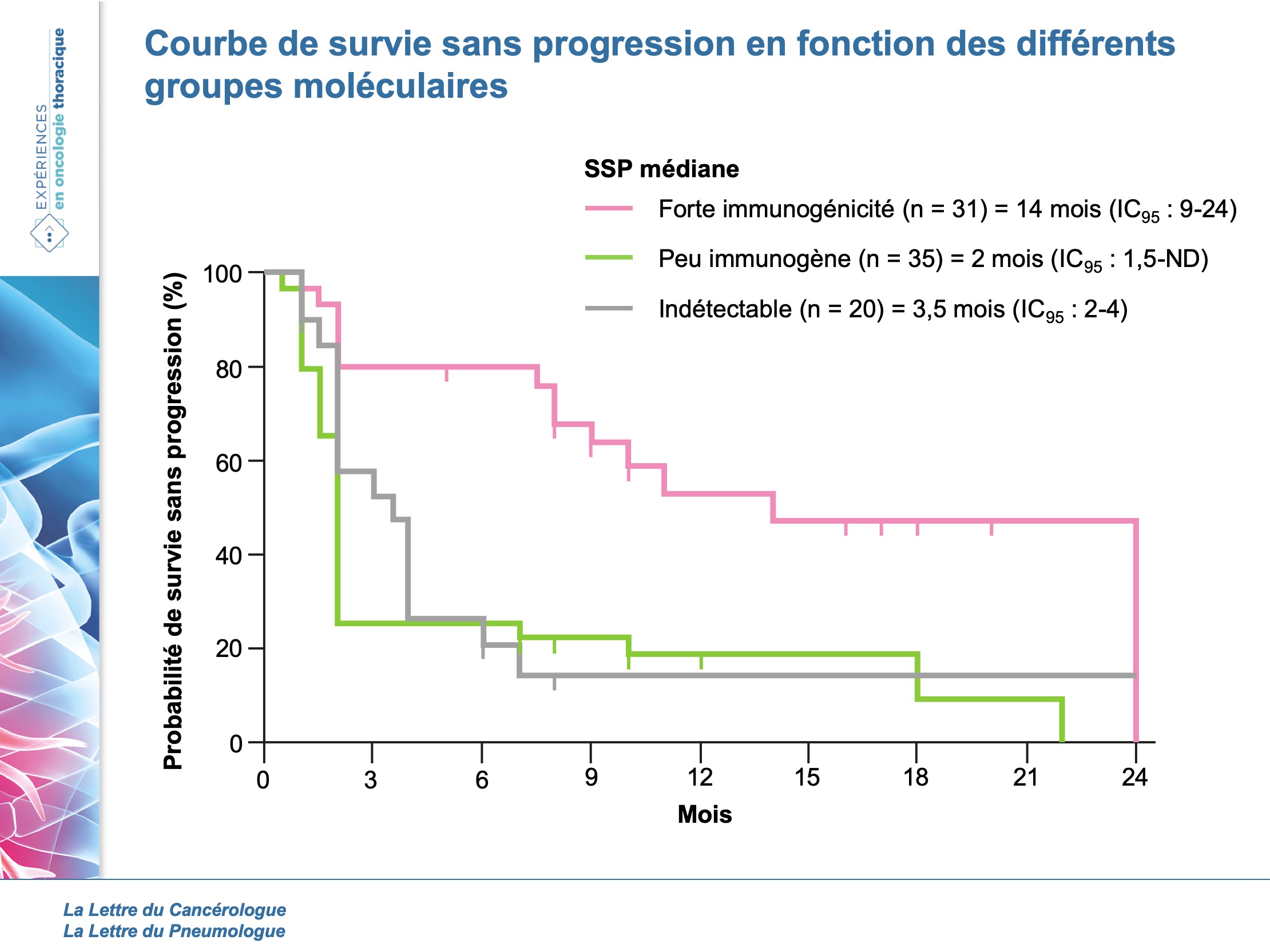
Par ailleurs, la diminution du ctDNA à 1 mois prédisait une meilleure réponse (SSP médiane 10 (IC95 : 8-18 mois)) que ceux présentant une augmentation (SSP médiane 2 (IC95 : 1,5-ND mois)).
Ce que cet article apporte à ma pratique :
- Ceci renforce mon sentiment d’un partenariat étroit avec l’anatomopathologie et la biologie moléculaire.
- Il faut rajouter dans notre panel NGS les mutations STK11 et PTEN et discuter la recherche des mutations transversion de KRAS et TP53.
- Peut-être ne pas proposer l’immunothérapie à des patients mutés STK11 ou PTEN en première intention.
- Cette étude m’encourage à utiliser le ctDNA qui semble plus représentatif de l’hétérogénéité spatiale et temporelle de la tumeur, même en dehors des patients ayant un driver oncogénique.
- La modification du ctDNA en cours de traitement pourrait permettre de mieux identifier les pseudoprogresseurs des vrais progresseurs.
Références
1. Guibert N et al. Targeted sequencing of plasma cell-free DNA to predict response to PD1 inhibitors in advanced non-small cell lung cancer. Lung Cancer 2019 Sep 6;137, doi 10.1016/j.lungcan.2019.09.005. [Epub ahead of print].
















