L’antibiothérapie débutée dans le mois précédant l’immunothérapie modifie-t-elle la réponse ?
Avec la découverte du microbiote, il semblerait que l’antibiothérapie débutée dans le mois précédant l’initiation des ICI, modifierait leur efficacité. Cette étude rétrospective multicentrique menée à Londres de 2015 à 2018 (1) essaie d’évaluer l’impact d’une antibiothérapie avant et pendant l’administration de l’immunothérapie sur la réponse au traitement et par conséquent la survie globale. Les auteurs ont sélectionné 196 patients d’un âge médian de 68 ans, dont 119 étaient atteints de CBNPC, 38 de mélanomes et 39 d’autres cancers. 67 % des CBNPC étaient des adénocarcinomes qui exprimaient un PD-L1 > 1 % dans 84 % des cas. La majeure partie de la cohorte (96 %) a reçu un anti-PD-1/PD-L1, dont 120 (62 %) en première ligne pour une durée médiane de 3,3 mois.
29 patients ont reçu une antibiothérapie dans le mois précédant le début du traitement (pATB), pour une durée de 7 jours ou moins dans 89 % et notamment des bêtalactamines (75 %).
68 patients ont reçu une antibiothérapie d’environ 7 jours durant le traitement (cATB), dont 57 % par bêtalactamines. La cause principale est une infection respiratoire dans 55 % des cas pour le groupe pATB et 85 % pour le groupe cATB.
Les analyses univariées confirment que le groupe pATB est associé à une moins bonne survie (HR = 7,4 [4,3-12,8] ; p < 0,001) contrairement au groupe cATB. Les patients du groupe pATB arrêtaient les ICI plus souvent pour cause de progression comme présenté dans la figure et le tableau.
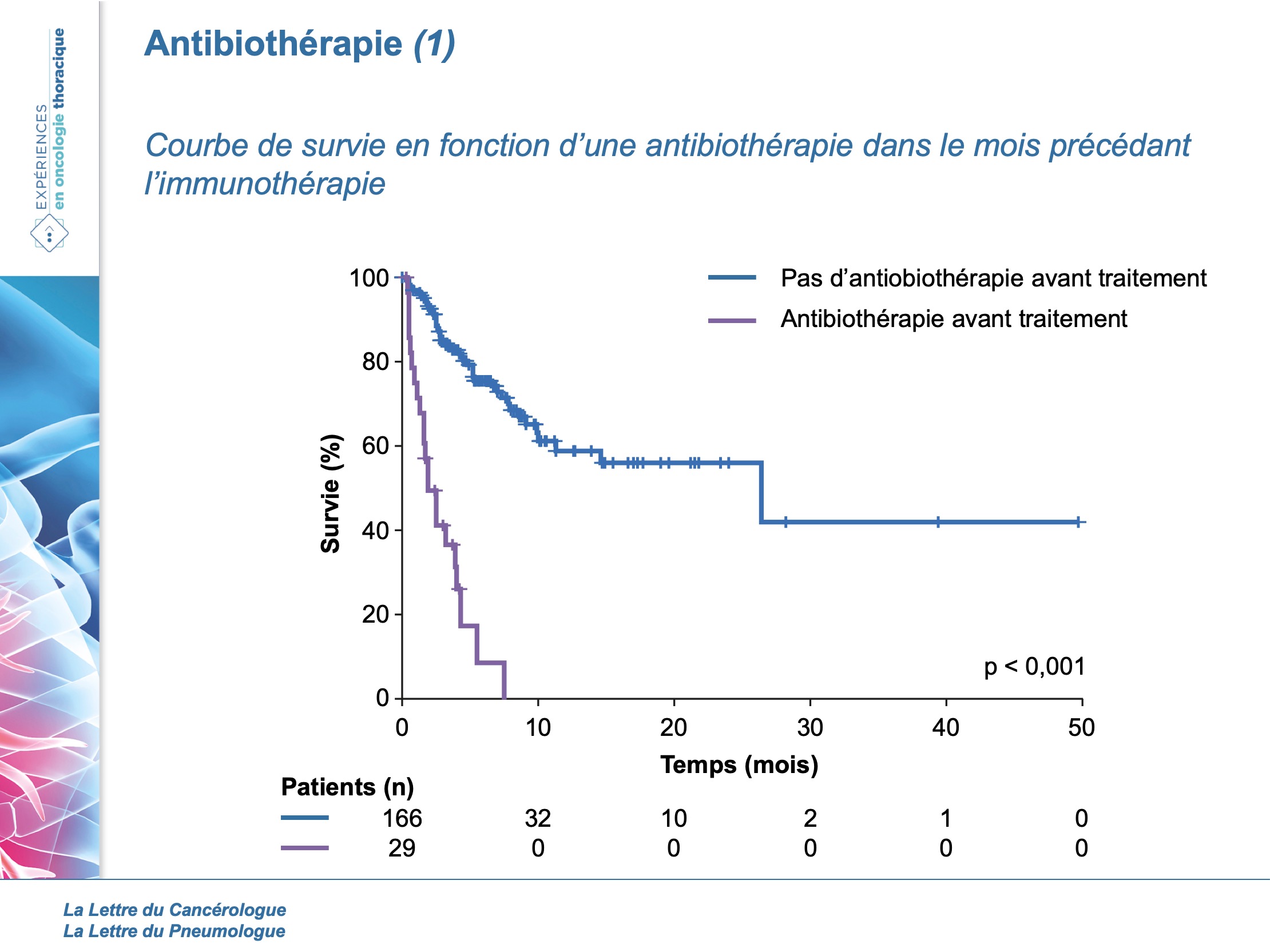
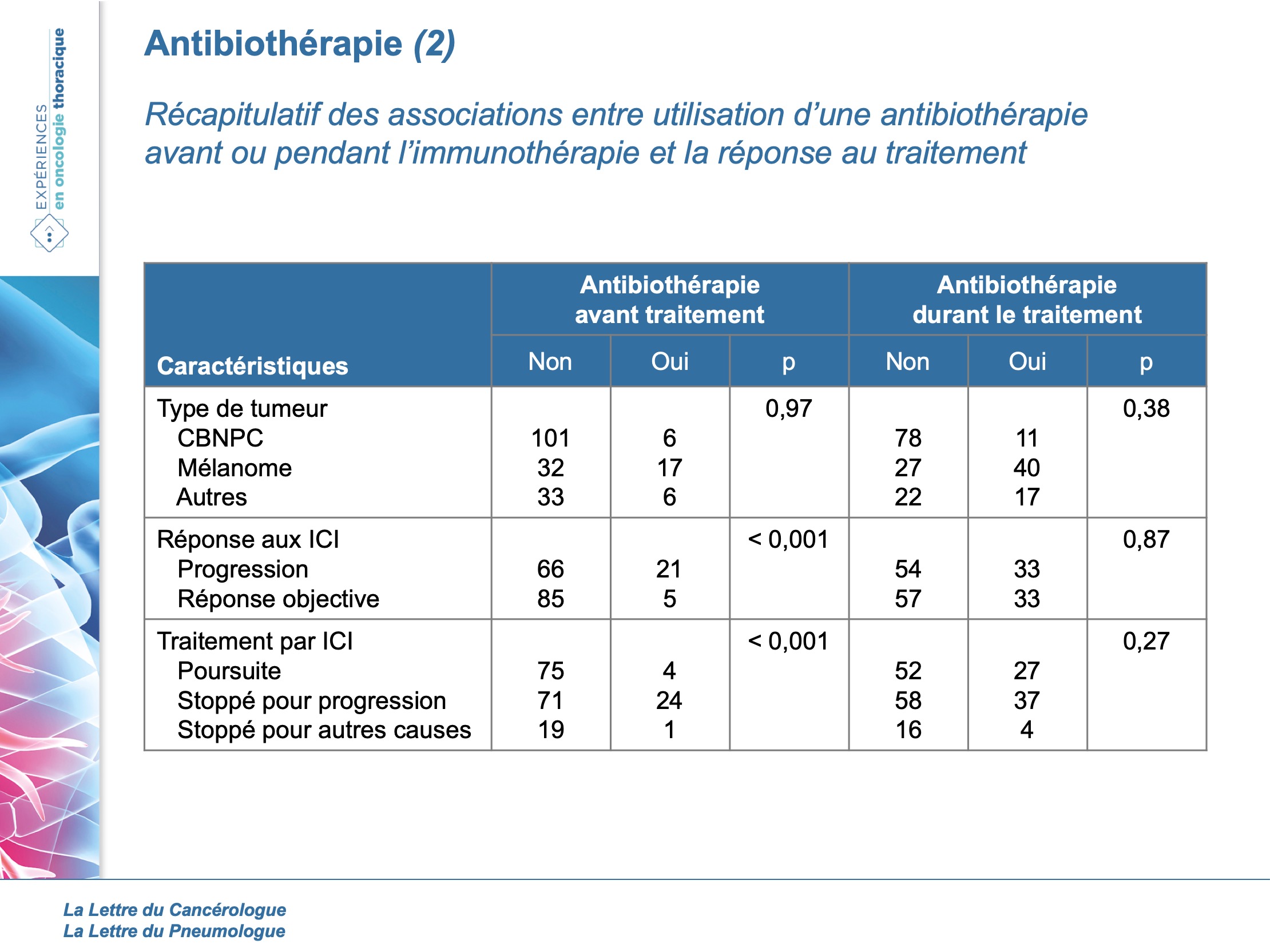
En séparant chaque cancer, pour s’affranchir des biais des différentes comorbidités (par exemple BPCO pour les CBNPC), le groupe pATB présente toujours une moins bonne survie : CBNPC (2,5 versus 26 mois ; HR = 9,3 [4,3-19]) ; mélanome (3,9 versus 14 mois).
De plus l’association entre une antibiothérapie dans le mois précédant le traitement et une plus mauvaise survie et réponse aux ICI était indépendante de la classe d’antibiotique, du PS, et surtout de l’utilisation de corticoïdes.
En conclusion, seule l’antibiothérapie dans le mois précédant l’administration d’une immunothérapie semble diminuer son efficacité et engendrer une moins bonne survie globale.
Ce que cet article apporte à ma pratique :
- Cette étude renforce des études précédentes (2, 3) qui n’avaient pas assez de puissance pour démontrer un impact d’une antibiothérapie avant ICI.
- Cette étude ne montre pas d’impact d’une antibiothérapie durant le traitement contrairement aux précédentes études rétrospectives.
- Cela rappelle de toujours peser le pour et le contre pour l’administration d’une antibiothérapie.
- Il faut probablement éviter une antibiothérapie dans le mois avant toute immunothérapie.
- Traquer les infections virales en utilisant les outils du quotidien.
Références
1. Pinato DJ et al. Association of prior antibiotic treatment with survival and response to immune checkpoint inhibitor therapy in patients with cancer. JAMA Oncol 2019 Sep 12. doi:10.1001/jamaoncol.2019.2785 [Epub ahead of print].
2. Galli G et al. Association between antibiotic-immunotherapy exposure ratio and outcome in metastatic non small cell lung cancer. Lung Cancer 2019;132:72-8.
3. Derosa L et al. Negative association of antibiotics on clinical activity of immune checkpoint inhibitors in patients with advanced renal cell and non-small-cell lung cancer. Ann Oncol 2018;29(6):1437-44.
















