Lorlatinib en première ligne dans les CBNPC ALK réarrangés
Le crizotinib (inhibiteur tyrosine kinase de première génération) a montré une supériorité en première ligne, dans les CBNPC présentant un réarrangement ALK, par rapport à la chimiothérapie. Depuis, des ITK de deuxième génération (alectinib, brigatinib, ensartinib) ont montré leur supériorité par rapport au crizotinib en première ligne. Cependant des mécanismes de résistance (mutations) et des progressions (notamment cérébrales) surviennent malgré ces traitements. Le lorlatinib est un nouvel ITK anti-ALK de troisième génération offrant une plus grande protection vis-à-vis des mutations de résistance et une meilleure pénétration encéphalique. Il a montré son efficacité dans des études de phase I-II en deuxième ligne après un traitement par un autre ITK anti-ALK. L’objectif de cet essai clinique était de montrer la supériorité du lorlatinib par rapport au crizotinib (traitement standard au moment du début de l’étude) en première ligne. Nous rapportons ici l’analyse intermédiaire planifiée (1).
Les critères d’inclusion étaient : âge > 18 ans, performans status 0-2, CBNPC localement avancé ou métastatique avec un réarrangement ALK en immunohistochimie, naïf de tout traitement systémique avec ou sans lésions cérébrales asymptomatiques (traitées ou non).
Les patients recevaient soit du lorlatinib 100 mg par jour ou du crizotinib 250 mg × 2 par jour par cycle de 28 jours avec une évaluation toutes les 8 semaines. L’objectif principal était la survie sans progression (SSP) selon un comité indépendant ; les objectifs secondaires étaient la SSP selon les investigateurs, la survie globale (SG), la réponse objective (RO) globale et cérébrale, et la tolérance.
Cette analyse intermédiaire portait sur les 296 patients inclus entre mai 2017 et février 2019. Les caractéristiques des deux groupes étaient équilibrées : femmes 60 % ; âge médian 60 ans ; non-fumeur/ancien fumeur 60 %/30 % ; adénocarcinome 95 % ; 27 % de métastases cérébrales dont 7 % ayant reçu de la radiothérapie.
Le groupe lorlatinib (n = 149) et le groupe crizotinib (n = 147) présentaient une SSP non atteinte et de 9,3 mois (IC95 : 7,6-11,1), respectivement (HR = 0,28 ; IC95 : 0,19-0,41) (figure 1). La RO était respectivement de 76 % versus 58 %.
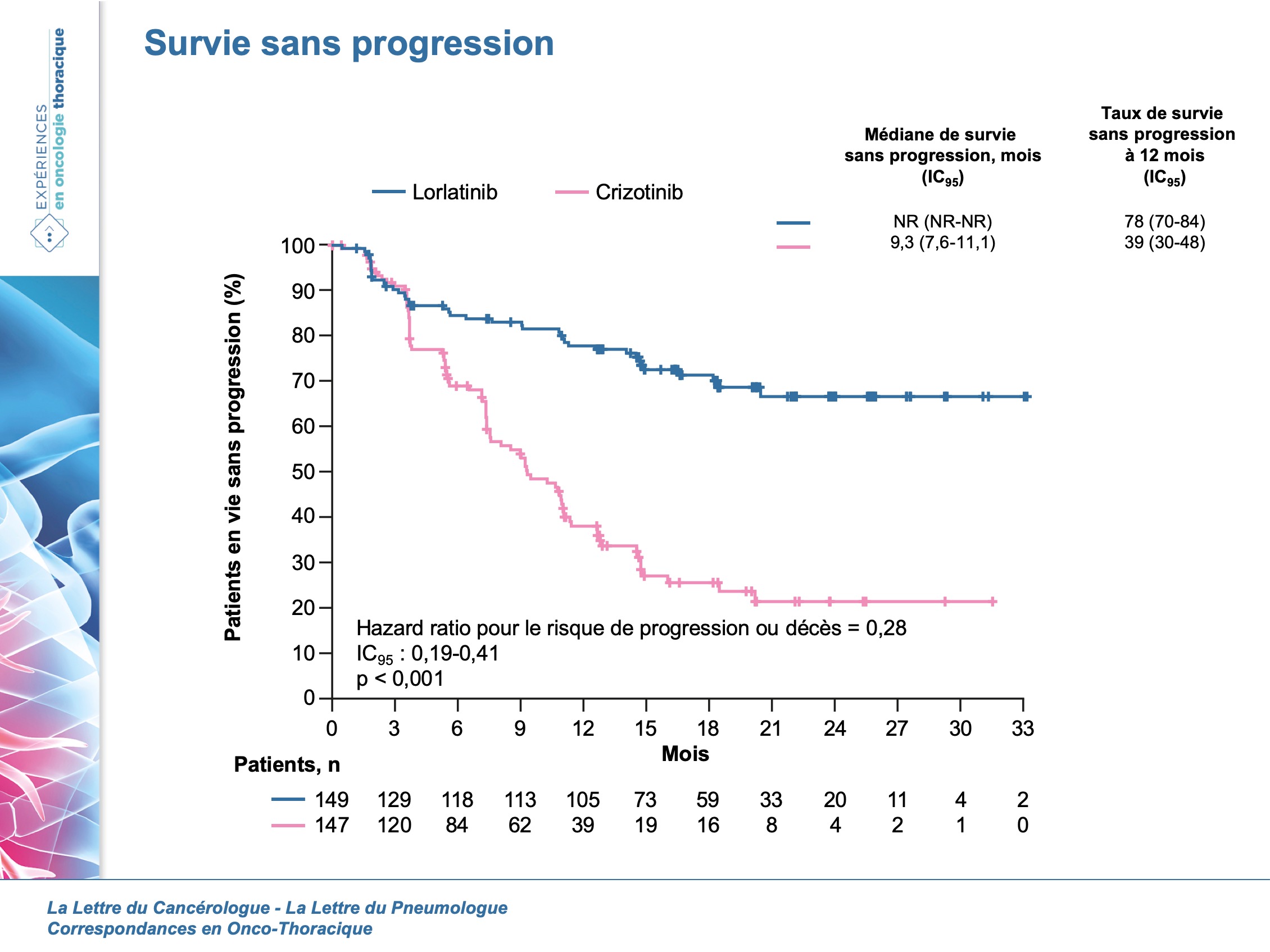
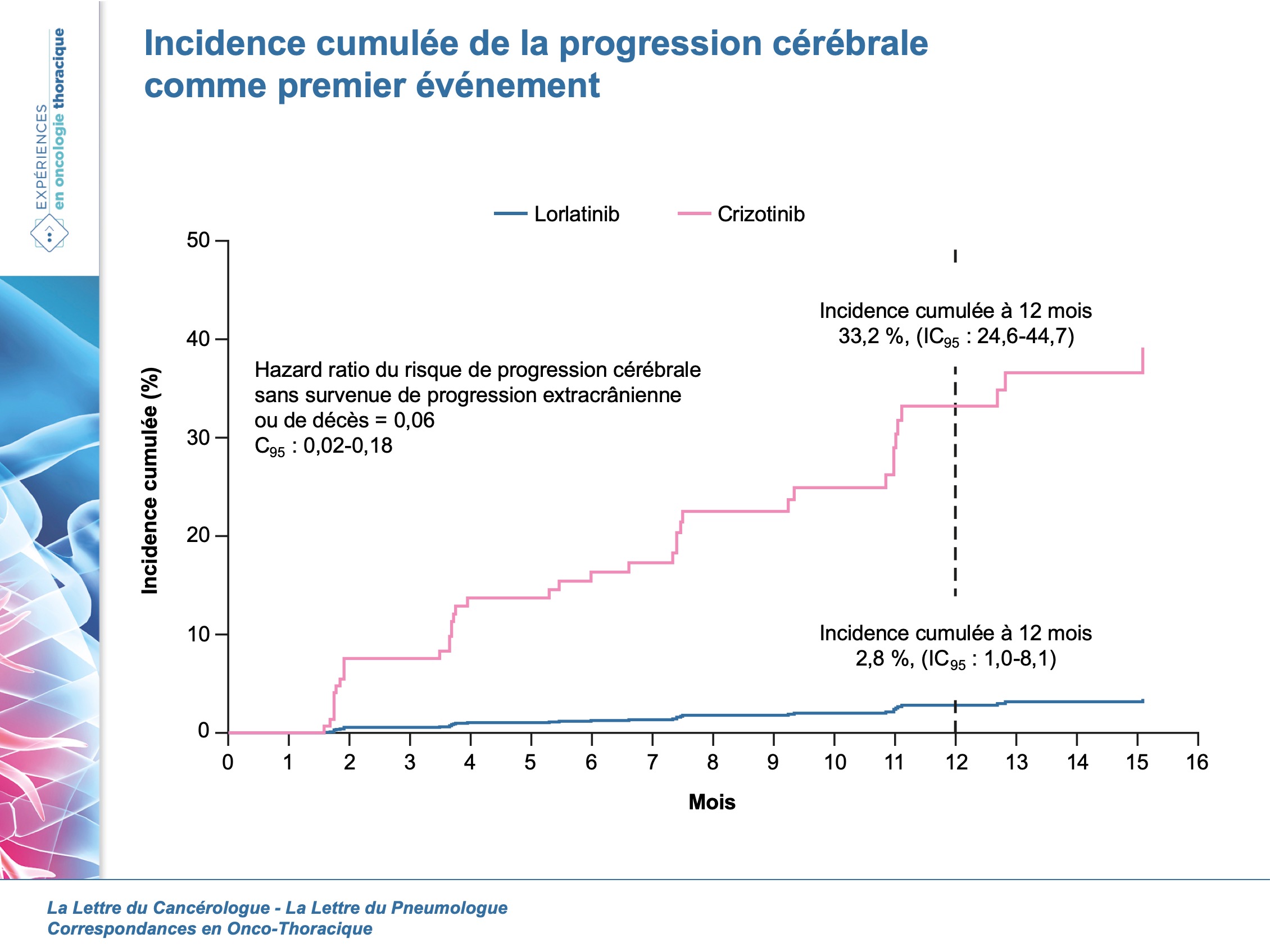
- Le lorlatinib semble très prometteur en première ligne, mais il faudra attendre des données matures pour la SSP (qui est aux alentours des 25 mois pour les ITK de seconde génération).
- La toxicité du lorlatinib est totalement différente des autres ITK avec surtout des dyslipidémies et des troubles cognitifs/humeurs.
- Ce traitement a une très bonne efficacité cérébrale et réduit le risque d’apparition de métastases cérébrales.
- Il est actuellement recommandé en deuxième ligne après un traitement par alectinib/céritinib.
Références
1. Shaw AT et al. First-line lorlatinib or crizotinib in advanced ALK-positive lung cancer. N Engl J Med 2020;383:2018-29.
















