Résultats finaux des études de phase II POPLAR et de phase III OAK : atézolizumab versus docétaxel dans les CBNPC prétraités
Les études de phase II POPLAR et de phase III OAK ont montré une amélioration significative de la survie globale avec l’atézolizumab versus docetaxel (p = 0,004 et p = 0,0003, respectivement) en deuxième ou troisième ligne de traitement d’un CBNPC au stade avancé d’histologie épidermoïde ou non épidermoïde. Cette étude [1] publiée en novembre 2020 rapporte les résultats finaux en termes de SG et de tolérance pour ces deux études. 287 patients ont été randomisés dans POPLAR (atézolizumab, 144 ; docétaxel, 143) et 1 225 dans OAK (atézolizumab, 613 ; docétaxel, 612). Les patients ont reçu de l’atézolizumab (1 200 mg dose fixe) ou du docétaxel (75 mg/m2) toutes les 3 semaines. Les résultats (figures) montrent que la SG est plus longue chez les patients ayant reçu de l’atézolizumab vs docétaxel dans POPLAR (médiane de SG à 12,6 mois vs 9,6 mois ; HR = 0,76 ; IC95 : 0,58-1,00) et dans OAK (médiane de SG à 13,3 mois vs 9,8 mois ; HR = 0,78 ; IC95 : 0,68-0,89). Les taux de survie à 4 ans dans POPLAR sont de 14,8 % (8,7-20,8) pour l’atézolizumab vs 8,1 % (3,2-13,0) pour le docétaxel. Ils sont respectivement de 15,5 % (12,4-18,7) et de 8,7 % (6,2-11,3) dans OAK. Le bénéfice de l’atézolizumab est retrouvé quels que soient l’expression de PD-L1 en IHC ou l’histologie (épidermoïde ou non-épidermoïde).
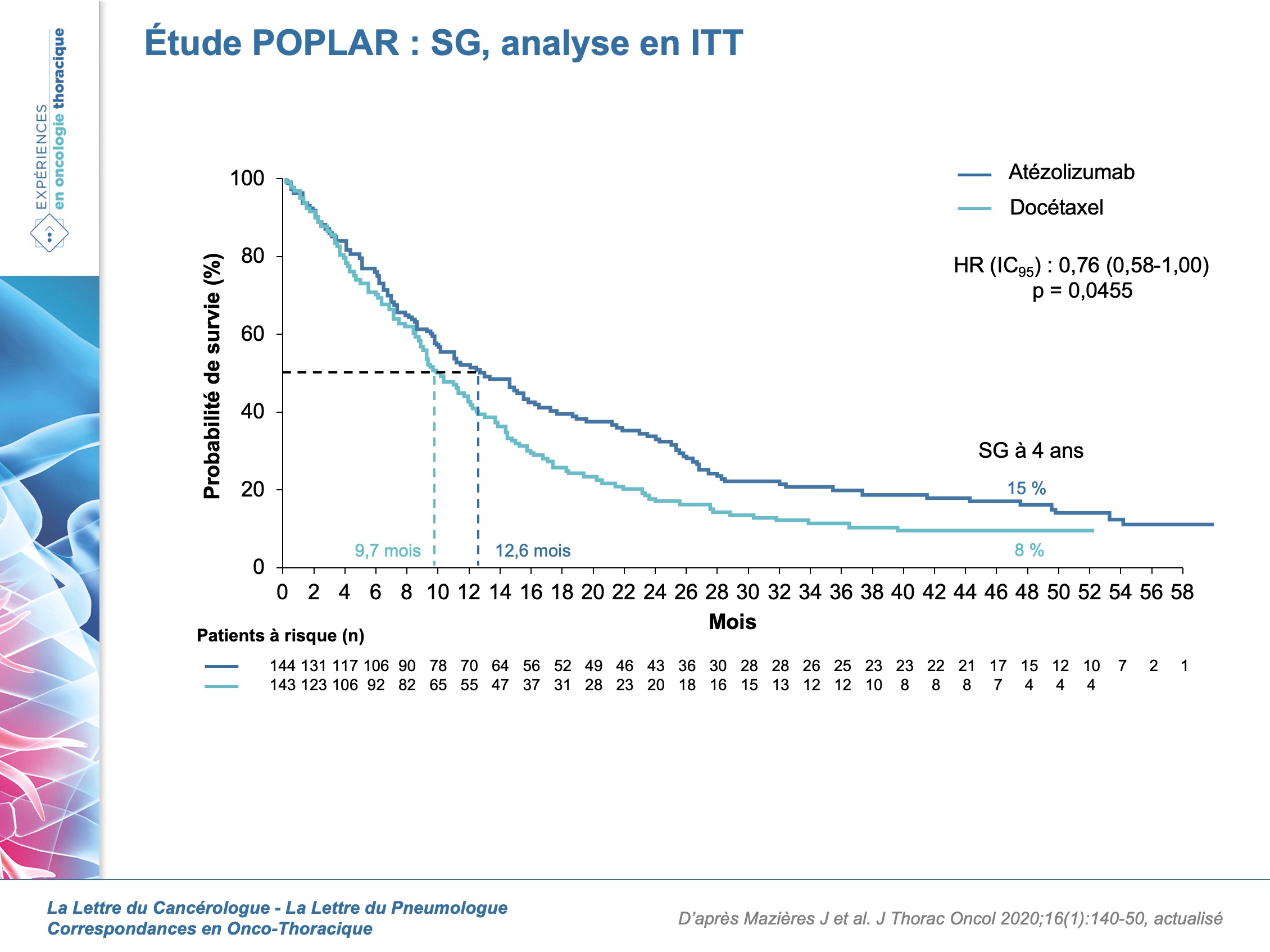
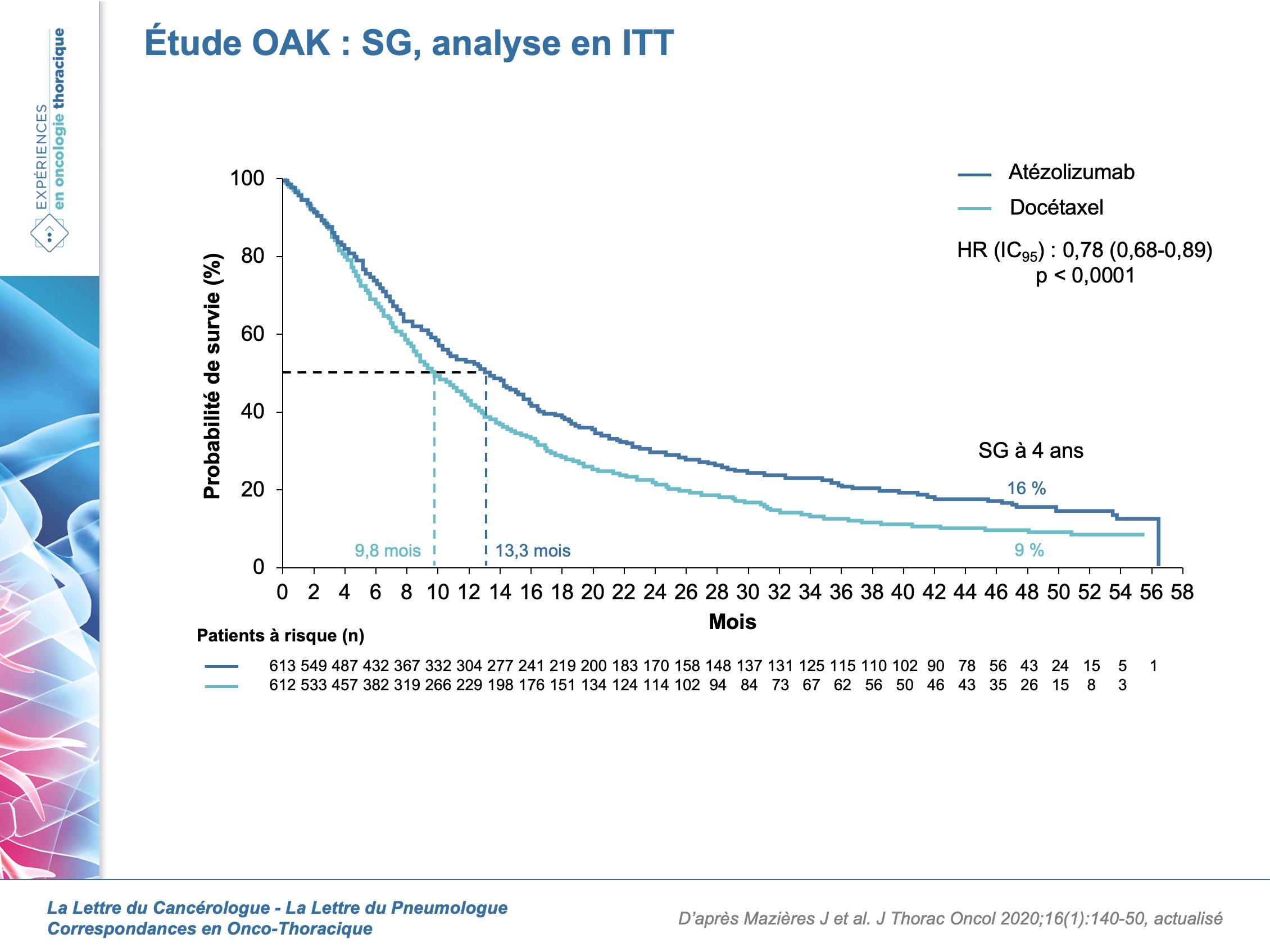
Plus le degré d’expression de PD-L1 est élevé, plus longue est la SG, ce qui a été retrouvé dans d’autres études avec l’atézolizumab (tableau).
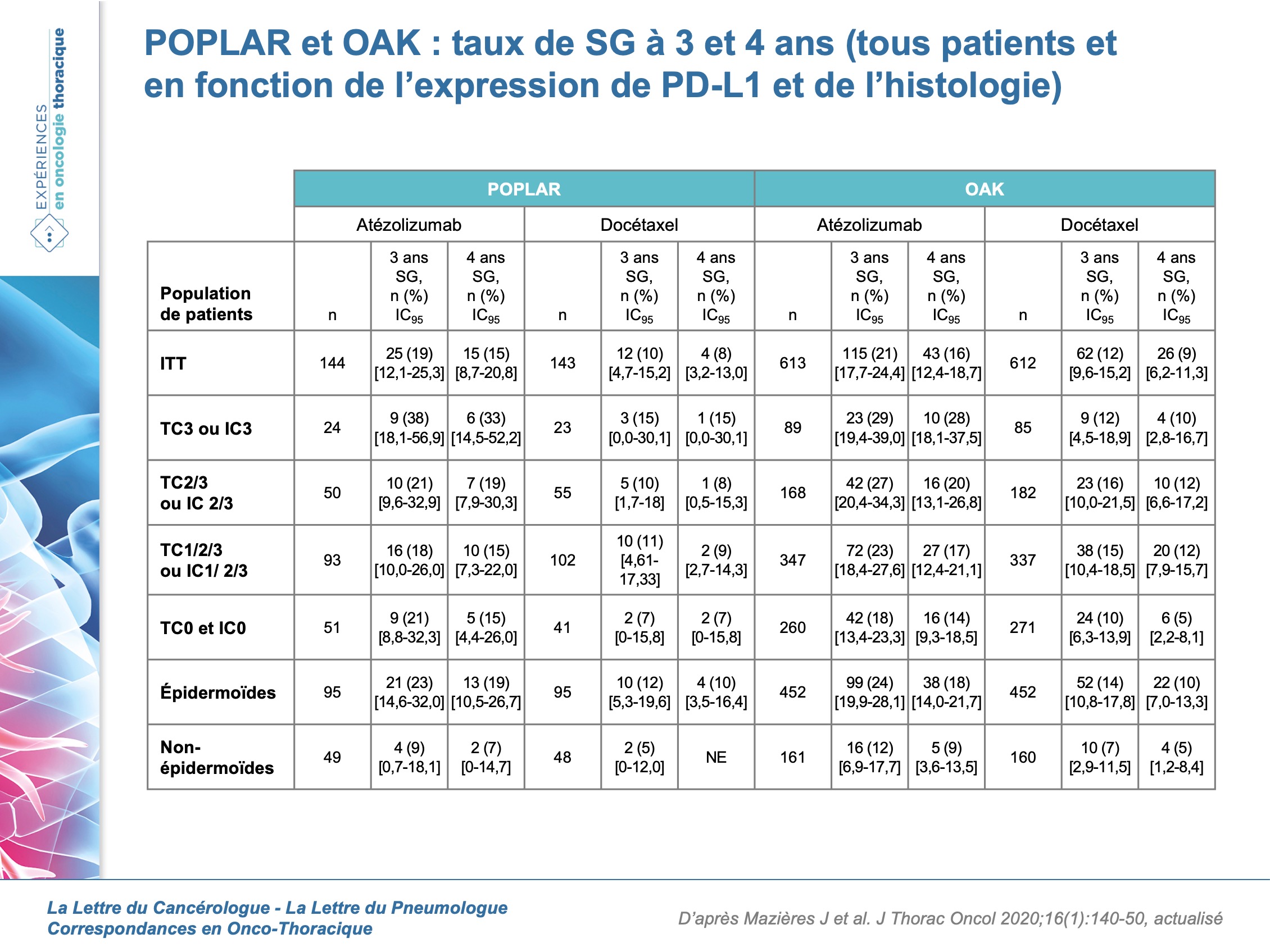
La plupart des patients survivants à 4 ans dans les bras docétaxel ont reçu une immunothérapie (50 % dans POPLAR et 65 % dans OAK). Chez les patients survivants à 4 ans, la plupart avaient un ECOG à 0 et une forme non épidermoïde ; environ la moitié étaient répondeurs (POPLAR : atézolizumab 7/15 ; docétaxel 3/4; OAK : atézolizumab 24/43 ; docétaxel 11/26). Le profil de tolérance est en faveur de l’atézolizumab avec un taux de toxicités de grade 3-4 liés au traitement moins important que sous docétaxel (respectivement 27 % et 16 % chez les patients survivants à 4 ans). Les principaux effets secondaires sous atezolizumab étaient une fatigue, des nausées, une perte d’appétit et une asthénie, essentiellement rapportés la 1re année de traitement. Les taux d’effets secondaires immuno-induits étaient bas : 1 % de pneumopathies de tous grades, moins de 1 % d’hépatites et de colites.
Ce que cet article apporte à ma pratique :
- Les études POPLAR et OAK démontrent la supériorité en termes de SG de l’anti-PD-L1 atézolizumab sur le docétaxel dès la 2e ligne de traitement.
- Le grand nombre de patients inclus, un bénéfice net quel que soit l’histologie (épiermoïdes/non épidermoïdes) et quel que soit le statut PD-L1 ainsi qu’un profil de tolérance très favorable sont indéniablement des points forts de ces études.
Références
1. Mazières J et al. Atezolizumab versus docetaxel in pretreated patients with NSCLC: final results from the randomized phase 2 POPLAR and phase 3 OAK clinical trials. J Thorac Oncol 2020;16(1):140-50.
















