Un régime de chimiothérapie dans la séquence thérapeutique des CBNPC ALK-positif ?
De nos jours les ITK anti-ALK de 2e génération se sont imposés, au lieu du crizotinib (1re génération), comme le standard de première ligne de traitement. Il s’agit notamment du céritinib (essai ASCEND-4), de l’alectinib (essai ALEX) et plus récemment le brigatinib (essai ALTA-1L) qui n’a pas encore l’AMM en France. Cependant, les patients développent inéluctablement des résistances, engendrant une progression. Ainsi, la question de la ligne post-ITK de 2e génération se pose, surtout depuis la publication de la phase II du lorlatinib montrant un taux de réponse objective de 40 % et une médiane de survie sans progression de 11 mois pour ceux ne présentant pas de mutations de résistance contre 4 mois pour ceux en ayant. Les auteurs se sont donc intéressés à l’efficacité d’une chimiothérapie (à base de sel de platine/pémétrexed) chez les CBNPC ALK-positif réfractaires à un ITK de 2e génération. Une étude rétrospective multicentrique a été réalisée sur 3 centres hospitaliers universitaires des États-Unis (1). Les patients inclus devaient avoir un CBNPC ALK-positif (détectés par FISH, NGS ou séquençage ARN ciblé) et avoir progressé après au moins un ITK anti-ALK de 2e génération (interdiction d’utiliser un ITK de 3e génération). La ligne de chimiothérapie de base devait comporter obligatoirement de sel de platine/pémétrexed (PT/pem), puis une autre thérapie pouvait être associée (bévacizumab, anti-PD-1/PD-L1, ITK anti-ALK). 58 patients ont été inclus dont 74 % n’ont jamais fumé, ils présentaient tous un adénocarcinome et avait un âge médian de 50 ans [22-75]. À noter que 31 patients (53 %) présentaient des métastases cérébrales à la progression, dont 5 avec une méningite carcinomateuse. Concernant le traitement antérieur, 88 % des patients ont reçu au moins 2 ITK anti-ALK, dont 57 % ont eu comme séquence crizotinib suivi d’un ITK de 2e génération. Pour le traitement par chimiothérapie : 32 (55 %) reçoivent du PT/pem ; 8 (14 %) du PT/pem + ITK anti-ALK ; 5 (8 %) du PT/pem + anti-PD-1/PD-L1 et 6 (10 %) du PT/pem + bévacizumab. Le délai médian entre la progression et le début de la chimiothérapie était de 24 jours. Le suivi médian était de 11 mois et le taux de réponse objective était de 29,7 % [15,9-47] et de 15,8% [3,4-39,6] parmi ceux qui avaient une atteinte cérébrale. La médiane de survie sans progression globale était de 4,3 mois [2,9-5,8] (figure 1) et le risque de développer une métastase cérébrale était de 30 % [18-44].
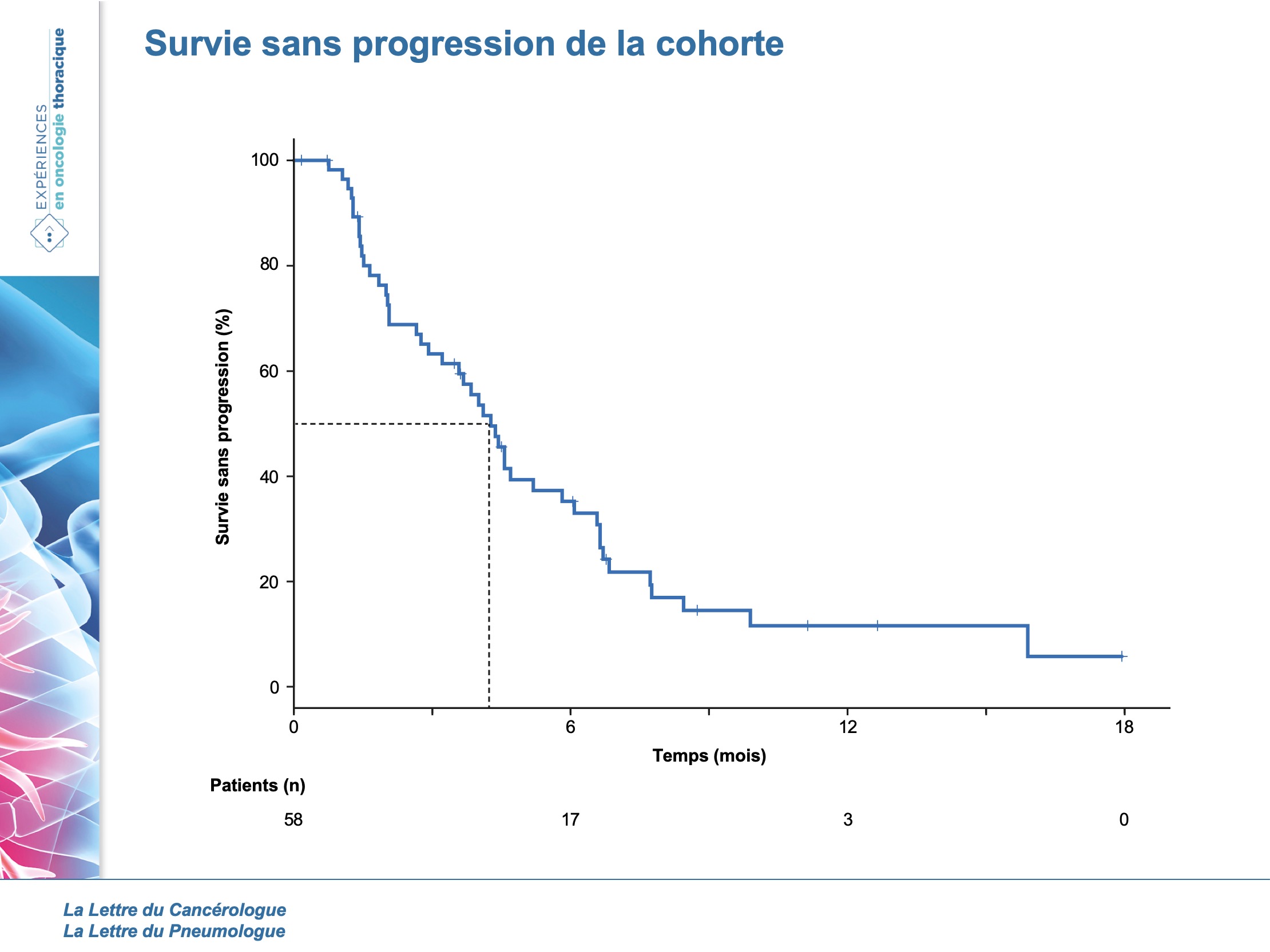
En comparant les sous-groupe PT/pem/bévacizumab et PT/pem/anti-PD-1 à celui ne comportant que PT/pem, ils ne retrouvent aucune différence significative en termes de survie sans progression. Néanmoins, entre le groupe PT/pem/ITK anti-ALK et PT/pem, il existe une différence significative de survie sans progression : 7,7 mois versus 3,6 mois (HR = 0,31 ; p = 0,002) respectivement (figure 2).
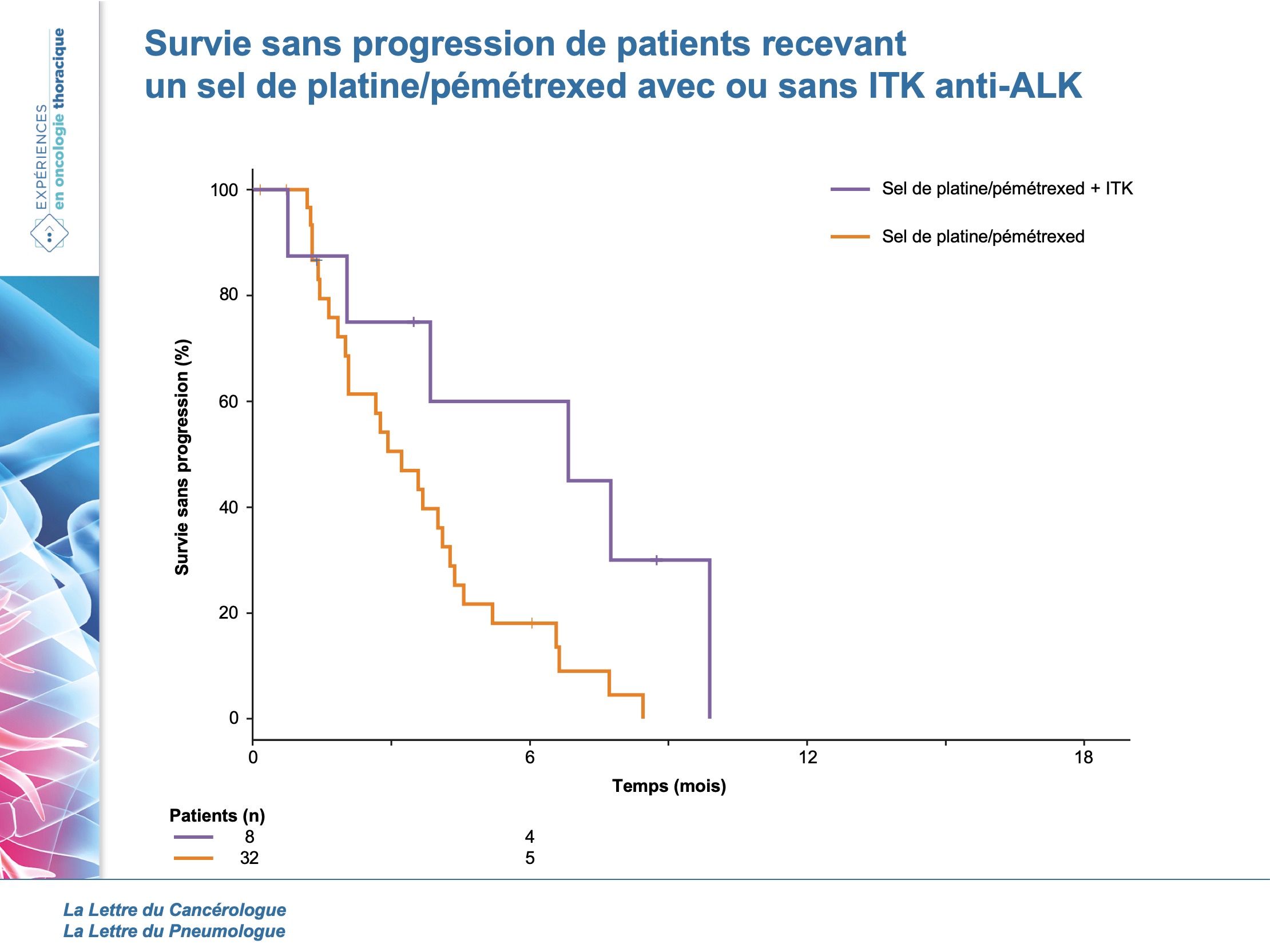
Les 2 groupes étaient similaires, sauf pour les atteintes cérébrales qui étaient plus fréquentes dans le groupe PT/pem. Néanmoins, l’incidence à un an de développer une métastase cérébrale était presque identique (28 % avec ITK anti-ALK versus 38 % sans). En conclusion, ils ont montré qu’une chimiothérapie à base de PT/pémétrexed a une activité après un ITK anti-ALK de 2e génération chez les CBNPC ALK-positif ne présentant pas de mutation ALK de résistance.
Ce que cela implique dans ma pratique :
- Ces résultats sont similaires à ceux obtenus avec le lorlatinib dans la même population (SSP médiane : 4 mois et taux de réponse objective : 31 %).
- Il faut donc proposer le lorlatinib s’il existe des mutations de résistance ALK (notamment…).
- En l’absence de mutation de résistance, le choix sera réalisé en prenant en compte les comorbidités et le désir du patient.
- Cela nous conforte à maintenir une thérapie anti-ALK si on réalise de la chimiothérapie.
- Il nous faut des essais prospectifs pour cette situation délicate.
Références
1. Lin JJ. et al. Efficacy of platinum/pemetrexed combination chemotherapy in ALK-positive non-small cell lung cancer refractory to second-generation ALK inhibitors. J Thorac Oncol 2019 Oct 26, doi 10.1016/j.jtho.2019.10.014 [Epub ahead of Print].
















