Étude TARGET-3D : efficacité d’un traitement de 6 semaines par GLE-PIB dans les hépatites C aiguës
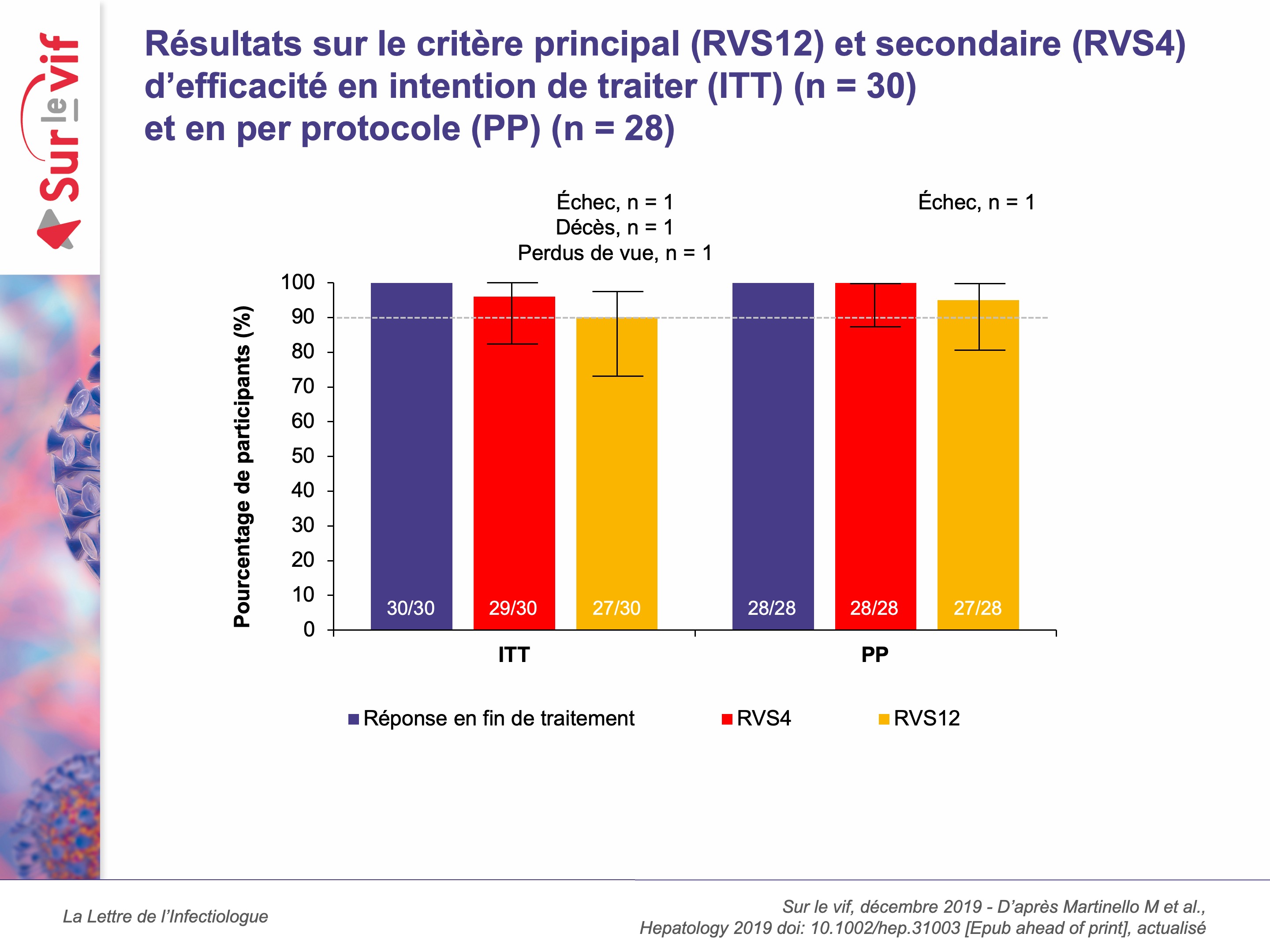
Chez les patients avec une infection chronique à VHC naïfs de traitement et non cirrhotiques, un traitement de 8 semaines par glécaprévir-pibrentasvir (GLE-PIB) – combinaison pangénotypique d’antiviraux directs – est recommandé. L’objectif de cette étude menée entre le 31 octobre 2017 et le 7 août 2018 (Australie, Royaume-Uni et Nouvelle-Zélande) était d’évaluer l’efficacité d’un traitement de 6 semaines par GLE-PIB chez des patients avec une infection à VHC aiguë et récente. Il s’agit d’une étude pilote, internationale, multicentrique à un seul bras menée en ouvert chez des adultes avec une infection à VHC récente (< 12 mois) qui ont reçu GLE-PIB 300 mg-120 mg une fois par jour pendant 6 semaines. La primo-infection à VHC était définie par la première détection d’un Ac anti-VHC et/ou ARN-VHC positif dans les 6 mois précédant l’inclusion et soit une hépatite C aiguë dans les 12 mois (séroconversion symptomatique ou ALAT > 10 × VLN), soit une séroconversion Ac anti-VHC dans les 18 mois. Les réinfections étaient quant à elles définies par un ARN-VHC positif dans les 6 mois précédant l’inclusion et des antécédents de clairance spontanée ou sous traitement. Le critère principal d’évaluation de l’étude était le taux de réponse virologique soutenue à 12 semaines post-traitement (RVS12). Au total, 30 hommes (âge médian 43 ans, 90 % d’HSH) ont été inclus : 77 % (n = 23) étaient co-infectés par le VIH, 47 % (n = 14) n’avaient jamais eu recours à l’injection de drogues par voie i.v. et une ré-infection a été documentée chez 13 % (n = 4) des patients. Le génotype 1 (GT1) était majoritaire (83 % ; n = 25) suivi par les GT4 (10 % ; n = 3) et GT3 (7 % ; n = 2). À l’inclusion, la durée médiane estimée de l’infection était de 29 semaines (extrêmes : 13-52) et l’ARN-VHC médian était de 6,2 log10 UI/mL (extrêmes 0,9-7,7). Les résultats (figure) sur le critère principal montrent qu’une RVS12 a été obtenue chez 90 % des patients (27/30) en analyse en ITT (96 % - 27/28 en per protocole). Un échec virologique a été constaté et 2 cas d’échec non virologique (1 décès et 1 perdu de vue). La tolérance du traitement a été excellente avec des effets indésirables tous d’intensité légère à modérée. Les résultats de cette étude avec une combinaison pangénotypique sur une durée courte sont donc positifs et demandent à être confirmés sur des effectifs plus importants.