Corticostéroïdes : faut-il les diminuer ou les arrêter avant l’immunothérapie ?
L’utilisation des corticostéroïdes au début d’une immunothérapie est associée à de mauvais résultats chez les patients atteints d’un cancer du poumon non à petites cellules (CPNPC), ce qui pose la question de savoir si l’administration des corticostéroïdes diminue l’efficacité de ces traitements. Cependant, les corticostéroïdes sont souvent prescrits pour soulager des symptômes liés au cancer qui sont associés indépendamment à un mauvais pronostic, et donc la survie plus courte observée n’est pas nécessairement le résultat d’un émoussement de la réponse immunitaire antitumorale liée aux corticostéroïdes.
Dans cet article, B. Ricciuti et al. (1) comparent les résultats cliniques chez 3 groupes de patients atteints d’un CPNPC :
- patients qui prenaient ≥ 10 mg de prednisone au début de l’immunothérapie pour des indications palliatives liées au cancer ;
- patients qui prenaient ≥ 10 mg de prednisone pour des indications non liées au cancer (exemple, traitement de maladies auto-immunes ou de poussée de BPCO) ;
- patients dont la dose de prednisone était < 10 mg.
Parmi 650 patients, 557 ont reçu 0-10 mg de prednisone, 66 ont reçu ≥ 10 mg de prednisone pour des indications palliatives liées au cancer et 27 ont reçu ≥ 10 mg de prednisone pour des indications non liées au cancer. Les caractéristiques cliniques des 3 groupes étaient bien équilibrées en termes d’âge, de sexe, d’histologie, de schéma thérapeutique, de statut mutationnel et d’expression de PD-L1. Les patients qui ont reçu ≥ 10 mg de prednisone pour des soins palliatifs liés au cancer étaient plus susceptibles d’avoir un mauvais performance status (PS) et d’avoir des métastases cérébrales. Les patients qui ont reçu ≥ 10 mg de prednisone pour des soins liés au cancer, comparativement aux patients qui ont reçu ≥ 10 mg de prednisone pour des indications non liées au cancer et aux patients recevant 0 à 10 mg de prednisone, ont obtenu un taux de réponses objectives plus faible (6,1 versus 22,2 versus 19,7 % ; p = 0,01) (figure 1A), avaient une survie sans progression médiane (SSPm) (1,4 versus 4,6 versus 3,4 mois ; p < 0,001) et une survie globale médiane (SGm) plus courtes (2,2 versus 10,7 versus 11,2 mois ; p < 0,001) (figure 1B). Les patients qui ont reçu ≥ 10 mg de prednisone pour des soins palliatifs liés au cancer ont présenté une SSPm significativement plus courte que les patients qui ont reçu 0 à 10 mg de prednisone (1,4 versus 3,4 mois ; p <0,001).
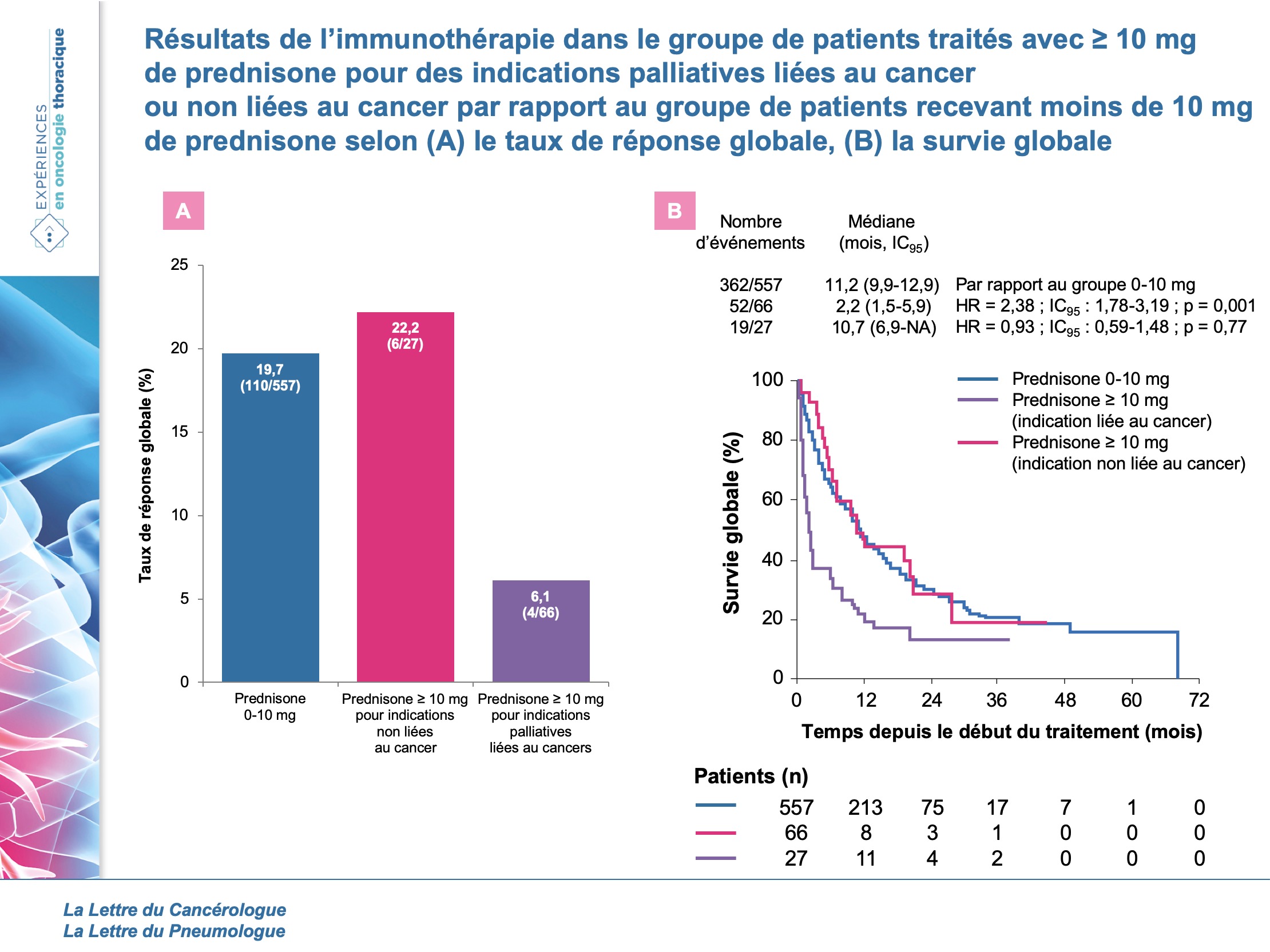
En revanche, aucune différence n’a été démontrée entre les patients ayant reçu 10 mg de prednisone pour des indications non liées au cancer et ceux ayant reçu une dose de 0 à 10 mg (4,6 versus 3,4 mois ; p = 0,24). De plus, la SGm était significativement plus courte chez les patients ayant reçu ≥ 10 mg de prednisone pour les soins palliatifs liés au cancer comparativement aux patients ayant reçu 0 à 10 mg (2,2 versus 11,2 mois ; p = 0,001). Cependant, il n’y avait pas de différence entre les patients qui avaient reçu 10 mg de prednisone pour des indications non reliées au cancer et ceux qui avaient reçu 0 à 10 mg (10,7 versus 11,2 mois ; p = 0,77).
Dans l’analyse multivariée, après ajustement par PS et statut PD-L1, l’utilisation de ≥ 10 mg de prednisone pour des indications liées au cancer était significativement associée à un risque accru de décès (HR = 1,60 ; IC95 : 1,07- 2,39 ; p = 0,02).
Cette étude confirme que l’utilisation de ≥ 10 mg de prednisone à l’instauration de l’immunothérapie pour un CPNPC était associée à un taux de réponse objective significativement plus faible, une SSP médiane plus courte et une SG médiane plus courte comparativement à l’utilisation de 0 à < 10 mg. Toutefois, les auteurs n’ont constaté aucune différence significative chez les patients ayant reçu ≥ 10 mg de corticostéroïdes pour des indications non reliées au cancer comparativement aux patients ayant reçu moins de 10 mg.
Ces données suggèrent que les corticostéroïdes ne devraient pas nécessairement être diminués ou interrompus avant le début de l’immunothérapie.
Ce que cet article apporte à ma pratique :
- L’utilisation des corticostéroïdes avant le début d’une immunothérapie est fortement débattue en raison des risques de réduction de l’efficacité.
- Les auteurs ont évalué l’impact des corticoïdes chez une cohorte de 650 patients atteints d’un CPNPC en fonction des doses et indications (palliatives ou non) de prednisone avant le début de l’immunothérapie.
- Les patients traités par ≥ 10 mg de prednisone pour des raisons liées au cancer en comparaison aux patients traités par ≥ 10 mg de prednisone pour des raisons non liées au cancer ou des doses entre 0 et 10 mg, avec un risque de décès plus important.
- Toutefois, aucune différence en termes de réponse et survie entre les patients traités par ≥ 10 mg de prednisone pour des raisons non liées au cancer et ceux traités avec des doses entre 0 et 10 mg.
- Cette étude confirme que l’utilisation de ≥ 10 mg de prednisone au moment de l’instauration de l’immunothérapie pour un CPNPC était associée à une réponse et une survie plus courtes comparativement à l’utilisation de 0 à 10 mg de prednisone, mais aucune différence significative n’a été retrouvée chez les patients ayant reçu ≥ 10 mg de corticostéroïdes pour des indications non reliées au cancer comparativement aux patients ayant reçu 0 à 10 mg de corticostéroïdes.
- Corticoïdes et IO : pas nécessairement incompatibles dans les CPNPC.
















